Городская больница анапы
Содержание:
- Элиминация
- Человек есть, а диагноза нет?
- Симптомы анемии
- Врожденный и приобретенный токсоплазмоз
- Виды анемии
- Трясет, знобит, колотит… Чья вина?
- Как свести неприятные ощущения к минимуму
- Деятельность ВОЗ
- Диагностика Малярии у детей:
- Лечение малярии
- Работа «Врачей без границ»
- Online-консультации врачей
- Что провоцирует / Причины Малярии у детей:
- Диагностика
- Морфологическая картина простейших при исследовании
- «Дары природы» — человеку
Элиминация
Элиминация малярии определяется как достигнутое в результате целенаправленных действий прерывание местной передачи конкретного вида малярийного паразита в пределах определенного географического района. Предотвращение возобновления передачи инфекции требует непрерывных усилий. Ликвидация малярии определяется как обеспечиваемое в результате целенаправленных действий постоянное поддержание на нулевой отметке глобальной заболеваемости малярией, вызываемой малярийными паразитами человека. Факт ликвидации малярии отменяет необходимость дальнейших противомалярийных мер.
География элиминации расширяется во всем мире, и все больше стран приближаются к цели сведения заболеваемости малярией к нулю. В 2019 г. число стран, зарегистрировавших менее 100 случаев местной передачи заболевания, составило 27, в то время как в 2000 г. таких стран насчитывалось 6.
Страны, в которых в течение как минимум трех лет подряд не было зарегистрировано ни одного местного случая малярии, соответствуют критериям для подачи заявки в ВОЗ на сертификацию элиминации малярии. За последние 20 лет Генеральным директором ВОЗ в качестве свободных от малярии было сертифицировано 10 стран: Объединённые Арабские Эмираты (2007 г.), Марокко (2010 г.), Туркменистан (2010 г.), Армения (2011 г.), Шри-Ланка (2016 г.), Кыргызстан (2016 г.), Парагвай (2018 г.), Узбекистан (2018 г.), Алжир (2019 г.) и Аргентина (2018 г.). Принятая ВОЗ Рамочная программа элиминации малярии (2017 г.) предусматривает полный набор инструментов и стратегий для достижения и поддержания элиминации.
Человек есть, а диагноза нет?
Именно в последнем случае диагноз сохраняется как ЛНГ. Это официальный термин, и включен он в МКБ-10 (международную классификацию болезней десятого пересмотра), поэтому врач, поставивший такой диагноз по результатам обследования, часто, к неудовольствию пациента, абсолютно прав. Разумнее оставить пациента под динамическим наблюдением, чем лечить его от придуманного хронического бронхита или пиелонефрита, зачастую абсолютно безуспешно, а то и во вред пациенту.
ЛНГ влечет за собой ряд проблем: неясность диагноза и, как следствие, — задержку лечения на неопределенный срок, длительность пребывания в стационаре, большой (часто дорогостоящий) объем обследований, утрату доверия пациента к врачу.
Симптомы анемии
Признаки патологии зависят от ее вида и степени тяжести. Легкая форма часто протекает бессимптомно. Возможны общая слабость, повышенная утомляемость, ослабление внимания. В тяжелых случаях (при понижении гемоглобина ниже 50 г/л) может развиться ацидоз (закисление крови), сердечная недостаточность.
К общим признакам, сопровождающим все виды анемии, принадлежат:
- головная боль, головокружение;
- летание «мушек» перед глазами;
- шум или звон в ушах;
- усиленное сердцебиение, одышка;
- сухость, шелушение и бледность кожи;
- понижение мышечного тонуса;
- резкая смена настроения, раздражительность;
- общая слабость, сонливость;
- понижение работоспособности, быстрая утомляемость.
Для железодефицитной формы характерны наличие трещин и заед в углах рта, поперечная исчерченность, слоистость и ломкость ногтей, сечение и выпадение волос, искажение вкусовых предпочтений (желание есть мел, землю), понижение артериального давления, обмороки.
При В12-дефицитной анемии человек ощущает покалывание и онемение в пальцах, чувство ползания мурашек, скованность и отечность конечностей, кожа приобретает желтоватый оттенок, а язык – малиновый, походка становится шаткой.
При апластическом малокровии в грудной области возникают колющие боли, физические усилия сопровождаются одышкой. На коже появляются мелкие кровоизлияния (петехии) в виде красной сыпи, кровоточат десны, менструации становятся длительными и обильными.
При фолиеводефицитной форме затрудняется пережевывание и глотание пищи, атрофируются слизистые оболочки ЖКТ, развивается непереносимость кислой пищи.
При постгеморрагической анемии кружится голова, понижаются давление и температура тела, учащается (но становится слабым) пульс, появляется холодный пот. Если кровотечение обильное, то возможны судороги, коматозное состояние и даже остановка сердца.
Для гемолитического малокровия характерны желтушность кожи и слизистых оболочек, потемнение мочи и кала, повышенная температура тела, увеличение размеров печени или селезенки.
При гипопластической форме усиливается кровоточивость десен, в ротовой полости образуются язвы, на коже появляются синяки, развивается тахикардия, постоянно хочется спать.
Врожденный и приобретенный токсоплазмоз
Различают врожденный токсоплазмоз и приобретенный токсоплазмоз. Врожденный токсоплазмоз, как понятно из его названия, поражает плод еще во время внутриутробного развития. Врожденный токсоплазмоз передается только от матери к плоду. Это крайне опасное заболевание, которое может привести к внутриутробной гибели плода, смерти новорожденного или тяжелым поражениям различных органов: нервной системы, глаз и т.д. Приобретенный токсоплазмоз менее опасен. Болезнь может протекать в острой или хронической форме. Острый приобретённый токсоплазмоз может протекать либо как заболевание, напоминающее тиф, с высокой температурой, увеличением печени, селезёнки, либо с преимущественным поражением нервной системы. В этом случае основными симптомами токсоплазмоза становятся головная боль, судороги, рвота, параличи и др.
Однако чаще приобретенный токсоплазмоз приобретает хроническое течение. При хроническом приобретенном токсоплазмозе, как правило, поднимается невысокая (субфебрильная) температура, возникает головная боль, увеличиваются печень и лимфоузлы, снижается работоспособность. Иногда хронический токсоплазмоз сопровождается поражением сердца, глаз, нервной системы и других систем и органов. У абсолютного большинства больных хронический токсоплазмоз протекает совершенно бессимптомно. Врожденный токсоплазмоз, как и приобретенный токсоплазмоз могут иметь рецидивирующее течение.
Несмотря на широкую распространенность заболевания, обязательные анализы на токсоплазмоз распространены отнюдь не повсеместно. В какой-то мере это связано с тем, что заражение здорового человека от больного токсоплазмозом невозможно. От человека к человеку заболевание токсоплазмоз передается исключительно «по вертикали», то есть от больной матери к будущему ребенку. Во всех остальных случаях заражение происходит при употреблении мясных продуктов, не прошедших достаточную термическую обработку, а также при контактах с кошками, которые и являются главными переносчиками и, как говорят биологи, «основным хозяином» токсоплазмы – возбудителя токсоплазмоза.
Нужно сказать также о том, что организм человека со здоровым иммунитетом довольно легко справляется с токсоплазмозом. И более того, выработанные организмом антитела к токсоплазмозу остаются у человека на всю жизнь, формируют стойкий иммунитет и не допускают рецидива заболевания. Действительной и серьезной проблемой токсоплазмоз становится при существенном снижении у человека иммунной защиты. Тяжелым заболеванием токсоплазмоз становится при ВИЧ-инфекции и других заболеваний, приводящих к снижению иммунитета (среди них герпес, цитомегаловирусная инфекция, инфекционный мононуклеоз и т.п.), при использовании угнетающих иммунитет препаратов, при облучении. Отдельно нужно сказать об опасности токсоплазмоза при беременности, когда возможна вертикальная передача токсоплазмоза (врожденный токсоплазмоз) от матери к плоду.
Виды анемии
В зависимости от причины различают 4 группы патологии:
- Дефицитная анемия – возникает при недостатке веществ, участвующих в процессе кроветворения.
- Постгеморрагическая анемия – вызвана острой или хронической потерей крови.
- Гемолитическая анемия – результат сокращения длительности жизни эритроцитов из-за усиленного разрушения.
- Гипопластическая, или апластическая, анемия (самая тяжелая форма) – развивается при нарушении кроветворной функции из-за ослабления способности костного мозга синтезировать кровяные клетки (эритроциты).
Известно несколько разновидностей дефицитной патологии:
- Железодефицитная анемия (встречается наиболее часто). Возникает при недостатке в организме железа, входящего в состав гемоглобина.
- В12-дефицитная анемия. Проявляется при дефиците витамина В12, необходимого для созревания эритроцитов и правильного функционирования нервной системы.
- Фолиеводефицитная анемия. Развивается при недостатке витамина В9 (фолиевой кислоты) в результате его недостаточного поступления в организм либо избыточного выведения.
Самые распространенные формы гемолитической анемии:
- Талассемия. Понижается скорость синтеза гемоглобина. К тому же он неполностью формируется, становится нестабильным, придает эритроцитам мишеневидную форму.
- Серповидно-клеточная анемия. В организме синтезируется дефектный гемоглобин, из-за чего эритроциты приобретают серповидный вид. Они разрушают друг друга острыми концами, повышают вязкость крови, закупоривают капилляры.
Вид анемии определяется врачом — терапевтом или гематологом на основе анализов крови.

Трясет, знобит, колотит… Чья вина?
Несколько подробнее остановимся на причинах ЛНГ.
Инфекционно-воспалительные заболевания — самый большой раздел, который включает в себя, помимо собственно инфекционных заболеваний, вызываемых бактериями, вирусами, простейшими, грибками, и гнойно-воспалительные заболевания внутренних органов, такие как абсцессы брюшной полости, заболевания почек, желчевыводящих путей. Многие инфекционные заболевания сегодня протекают не так как десятилетия назад. В век антибиотиков, изменившейся экологии, модифицируются, приспосабливаясь к новым условиям и микроорганизмы. Вновь актуален туберкулез, который протекает не с изменениями в легких, а поражает другие внутренние органы, кости, лимфатические узлы, часто проявляясь лишь длительной лихорадкой. Забытая одно время болезнь – малярия — вновь заявила о себе лихорадкой. Только лихорадкой могут проявляться вирусные заболевания – герпес, мононуклеоз (вирус Эпштейн-Барр), гепатиты В и С, вирус иммунодефицита человека. В связи с активизацией иксодовых клещей участились заболевания лаймской болезнью, вызванной боррелией, которая передается при укусе клеща.
Среди опухолей лихорадками чаще манифестируют заболевания крови или гемобластозы, в частности, лимфопролиферативные заболевания (лимфогранулематоз, лимфосаркома), однако и опухоли различных органов могут сопровождаться лихорадкой.
Системные заболевания соединительной ткани (системная красная волчанка, ревматоидный артрит, системные васкулиты и другие) — большая группа заболеваний, при которых процесс может начинаться именно с лихорадки. В этих случаях нередко требуется длительное динамическое наблюдение, повторные лабораторные обследования.
Прочие патологии включают в себя разнообразные по этиологии заболевания кишечника, легких, печени, щитовидной железы, сосудов, а также аллергические заболевания, в том числе, и лекарственные лихорадки, возникающие в ответ на прием различных препаратов. Кроме того, существует группа наследственных заболеваний, проявляющихся в зрелом возрасте лихорадкой.
Как свести неприятные ощущения к минимуму
Начинать использовать противогерпесные препараты необходимо начать, как только вы почувствовали пощипывание. Лекарства не избавят Вас от вируса, но позволят остановить его развитие и ускорить выздоровление. Существуют препараты, предотвращающие развитие вируса: таблетки, мази для наружного применения, которые помогают заживлению пузырьков и язв, уменьшению неприятных ощущений.
При нанесении мази используйте ватные палочки, что бы избежать передачу вируса с губ на кожу пальцев.
Герпес требует внимания специалистов! «Простуда» на губах может оказаться симптомом серьезных заболеваний: резкого снижения иммунитета, онкологических заболеваний, ВИЧ-инфекции.
Если Вас мучают рецедивы герпеса – обратитесь к врачу. Специалист не только избавит Вас от лишних волнений и исключит опасность для здоровья, но и поможет подобрать комплексную программу профилактики и лечения герпеса.
Для того, чтобы записаться к врачу-иммунологу или дерматологу по программе диагностики и лечения герпеса, позвоните в клинику «Семейный доктор» +7 (495) 775 75 66 (время работы клиники: пн-пт с 8.00 до 21.00, сб-вс с 9.00 до 20.00), либо запишитесь на прием и диагностику через форму
Деятельность ВОЗ
Глобальная техническая стратегия ВОЗ по борьбе с малярией на 2016‑2030 гг.
Принятая Всемирной ассамблеей здравоохранения в мае 2015 г. Глобальная техническая стратегия ВОЗ по борьбе с малярией на 2016-2030 гг. задает технические параметры работы во всех эндемичных по малярии странах. Она призвана направлять и обеспечивать поддержкой региональные и национальные программы в ходе их работы по противодействию малярии и достижению ее элиминации.
Эта стратегия ставит далеко идущие, но достижимые глобальные задачи, включая:
- сокращение к 2030 г. заболеваемости малярией не менее чем на 90%;
- сокращение к 2030 г. показателей смертности от малярии не менее чем на 90%;
- элиминацию малярии не менее чем в 35 странах к 2030 г.;
- предупреждение повторного появления малярии во всех свободных от малярии странах.
Данная стратегия явилась результатом широкого консультативного процесса, продолжавшегося два года с участием более 400 технических экспертов из 70 государств-членов.
Глобальная программа по борьбе с малярией
Глобальная программа ВОЗ по борьбе с малярией обеспечивает координацию международных усилий ВОЗ по борьбе с малярией и достижению ее элиминации посредством:
- разработки норм, стандартов, политики, технических стратегий и руководящих принципов, информирования о них и содействия их принятию;
- независимой оценки глобального прогресса;
- разработки подходов для укрепления потенциала, совершенствования систем и ведения эпиднадзора;
- выявления факторов, угрожающих эффективной борьбе с малярией и ее элиминации, а также поиска новых направлений деятельности.
Поддержку и консультативную помощь Программе оказывает Консультативный комитет по политике в отношении малярии (ККПМ), состоящий из экспертов по малярии, назначенных в ходе открытого выдвижения кандидатур. Мандат ККПМ заключается в том, чтобы предоставлять стратегические рекомендации и технические заключения по всем аспектам борьбы с малярией и ее элиминации в рамках транспарентного, гибкого и пользующегося доверием нормотворческого процесса.
«Тяжелое бремя требует высокой эффективности»
В мае 2018 г. на сессии Всемирной ассамблеи здравоохранения Генеральный директор ВОЗ д‑р Тедрос Адханом Гебрейесус призвал использовать новый инициативный подход для ускорения прогресса в борьбе с малярией. Реализация новой инициативы «Тяжелое бремя требует высокой эффективности», выполняемой при активном участии стран, была начата в ноябре 2018 г. в Мозамбике.
В настоящее время в ее осуществлении принимают участие 11 стран с самым тяжелым бременем болезни (Буркина-Фасо, Камерун, Демократическая Республика Конго, Гана, Индия, Мали, Мозамбик, Нигер, Нигерия, Уганда и Объединенная Республика Танзания). Основными элементами инициативы являются:
- мобилизация политической воли для сокращения бремени малярии;
- предоставление информации стратегического характера для достижения реальных изменений;
- совершенствование руководящих принципов, политики и стратегий;
- скоординированные меры борьбы с малярией на национальном уровне.
В основе инициативы «Тяжелое бремя требует высокой эффективности», выполняемой при активном участии ВОЗ и партнерства ОВМ по искоренению малярии, лежит принцип, согласно которому никто не должен умирать от болезни, поддающейся профилактике и диагностике и полностью излечимой при помощи существующих лекарственных средств.
Диагностика Малярии у детей:
Самый простой вариант диагностики – когда у ребенка периодически повторяются приступы (с ознобом, потами и жаром), приступы гипохромной анемии, увеличены печень и селезенка, появляется субиктеричность кожи и склер.
Диагностика малярии у младенцев затруднена
Врачу важно знать о пребывании больного малыша в эндемическом очаге малярии. Для окончательного диагноза необходимы лабораторные исследования – в периферической крови обнаруживают возбудителя малярии
Кровь для исследования лучше брать во время приступа, но можно и во внеприступном периоде.
Для серологической диагностики используют РИФ (чаще всего), РНГА и реакцию энзиммеченных антител (РЭМА). В качестве антигенов в РИФ берут препараты крови, содержащие много шизонтов. РИФ становится положительной на 2 неделе эритроцитарной шизогонии.
Малярию при диагностике дифференцируют с возвратным тифом, бруцеллезом, гемолитической желтухой, висцеральным лейшманиозом, сепсисом, лейкозом, циррозом печени, туберкулезом и т. д. Малярийную кому дифференцируют с коматозными состояниями, возникающими при брюшном тифе, вирусном гепатите В, менингоэнцефалите, реже при гнойном менингите.
Лечение малярии
Показанием для госпитализации является не только точно установленный диагноз малярии, но и подозрение на малярию. Для ликвидации приступов малярии назначают гематошизотропные препараты из группы 4-аминохинолинов (хингамин, гидроксихлорохины), а также плаквенил, бигумаль, хлоридин, мефлохин и хинин. Указанные средства обеспечивают радикальное излечение только тропической и четырехдневной малярии. После ликвидации приступов трехдневной и овале-малярии необходимо противорецидивное лечение примахином или хиноцидом.
Специфическое лечение начинают фазу после установления диагноза. Чаще всего применяют хингамин (делагил) внутрь после еды. Курсовая доза для взрослого 2—2,5 г. Лечение проводят 3 дня. Суточная доза в первый день 1 г. При тропической малярии назначают дополнительно 0,5 г хингамина, а курс лечения может быть продлен до 4—5 дней. Примахин принимают внутрь после еды. Суточную дозу 0,027 г делят на 1—3 приема. Продолжительность курса 14 дней. В связи с широким распространением хлорохинустойчивых штаммов P. falciparum основным этиотропным средством лечения тропической малярии при тяжелом течении является хинин. Разовая доза для взрослых 10 мг/кг, суточная — не более 2 г (1 мл 50% раствора хинина разводят в 500 мл изотонического раствора натрия хлорида). Препарат вводится внутривенно очень медленно, капельно. После улучшения состояния больного проводят курс лечения делагилом; если штамм Р. falcipaniro хлорохинустойчив — фансидаром, метакельфином, тетрациклином.
При развитии осложнений наряду со специфической терапией проводят патогенетическое лечение, которое при малярийной коме направлено на устранение отека головного мозга, уменьшение проницаемости сосудистых стенок, уменьшение гипоксии, нормализацию водно-электролитного обмена. Для дезинтоксикации вводят внутривенно 500—1000 мл реополиглюкина, преднизолон по 30—60 мг 3 раза в сутки, назначают антигистаминные препараты, вводят 40—80 мг фуросемида. При гемоглобинурийной лихорадке отменяют прежде всего препарат, вызвавший гемолиз. Назначают кортикостероиды, растворы глюкозы, натрия хлорида, вводимые внутривенно, по показаниям переливают плазму или эритроцитную массу. При развитии острой почечной недостаточности проводится гемодиализ.
За реконвалесцентами устанавливается диспансерное наблюдение в течение 2 лет. Врач кабинета инфекционных заболеваний поликлиники ежемесячно в период с мая по сентябрь и один раз в 3 месяца в остальное время года производит осмотр реконвалесцента и при подозрении на наличие рецидива назначает анализ крови с целью выявления малярийных плазмодиев.
Прогноз при своевременной и правильной терапии благоприятный. В большинстве случаев малярия заканчивается полным выздоровлением. Летальность составляет в среднем 1%. Летальные исходы в подавляющем большинстве случаев наблюдаются при осложненном течении тропической малярии.
Работа «Врачей без границ»
В 2016 году MSF оказала помощь в лечении 2,5 миллионов случаев заболевания малярией. С 2001 года ВОЗ рекомендует использование комбинированной терапии на основе артемизинина для лечения заболевания. За последние 15 лет использование новых методов лечения способствовало значительному снижению числа смертей, связанных с малярией.
Тем не менее, в нескольких регионах была зафиксирована устойчивость к артемизинину, вызванная по крайней мере, частично, применением монотерапии (использование артемизинина без комбинации с другими препаратами), поддельных и некачественных препаратов, а также из-за прерывания лечения при ослаблении проявлений болезни.
Ситуация может усугубиться и создать более серьезную угрозу и для общественного здравоохранения, поскольку в ближайшие несколько лет не будет найдено замены терапии, на основе артемизинина. В Камбодже, где рост устойчивости к артемизинину представляет особую угрозу, MSF изучает способы распространения лекарственно-устойчивой малярии и оценивает, какая из стратегий может способствовать искоренению болезни в этом районе.
В 2012 году, команды MSF провела в Мали и Чаде первую широкомасштабную сезонную кампанию по химиотерапии малярии (КХМ), предоставляя превентивное лечение малярии детям в тех местах, где болезнь широко распространена из-за системного применения антималярийных препаратов.
В настоящее время MSF внедряет эту стратегию в пяти странах; в 13 странах региона Сахель в Африке c высоким уровнем восприимчивости во время сезонного всплеска заболевания она уже была интегрирована в национальную программу здравоохранения. Более 15 миллионов детей пройдут профилактику в 2016 году. Однако предполагается, что данная стратегия не станет постоянным инструментом в борьбе с заболеванием.
Защитный эффект терапии – относителен и имеет ограниченный срок действия, всего несколько недель после завершения лечения. Таким образом, терапия — важный подход к спасению жизни в некоторых ситуациях, которые, однако, не отменяют необходимость в системных, долгосрочных решениях этого вопроса.
‘RTS,S’ — первая вакцина против малярии, прошедшая клинические испытания после многолетних исследований. Тем не менее, ее эффективность ограничена, особенно в отношении тяжелых форм заболевания, также она сложна в применении. При лечении необходим прием четырех доз, две из них необходимо принять спустя 18 месяцев после первых двух.
Дальнейшие пилотные исследования с участием этой вакцины начнутся в 2018 году, их проведут сторонние организации. MSF по-прежнему призывает к продолжению разработки безопасной, действенной и недорогой вакцины, которую будет легко использовать в развивающихся странах.
Online-консультации врачей
| Консультация андролога-уролога |
| Консультация специалиста по лазерной косметологии |
| Консультация специалиста по лечению за рубежом |
| Консультация психолога |
| Консультация нейрохирурга |
| Консультация нарколога |
| Консультация гастроэнтеролога |
| Консультация пульмонолога |
| Консультация невролога |
| Консультация офтальмолога (окулиста) |
| Консультация пластического хирурга |
| Консультация эндокринолога |
| Консультация трихолога (лечение волос и кожи головы) |
| Консультация хирурга |
| Консультация диетолога-нутрициониста |
Новости медицины
Футбольные фанаты находятся в смертельной опасности,
31.01.2020
«Умная перчатка» возвращает силу хвата жертвам травм и инсультов,
28.01.2020
Назван легкий способ укрепить здоровье,
20.01.2020
Топ-5 салонов массажа в Киеве по версии Покупон,
15.01.2020
Новости здравоохранения
Глава ВОЗ объявил пандемию COVID-19,
12.03.2020
Коронавирус атаковал уже более 100 стран, заразились почти 120 000 человек,
11.03.2020
Коронавирус атаковал 79 стран, число жертв приближается к 3200 человек,
04.03.2020
Новый коронавирус атаковал 48 стран мира, число жертв растет,
27.02.2020
Что провоцирует / Причины Малярии у детей:
Возбудитель — малярийный плазмодий — относится к типу простейших, роду плазмодиев. Существует 4 вида возбудителей малярии у ребенка: P. malariae, P. vivax, P. falciparum, P. ovale.
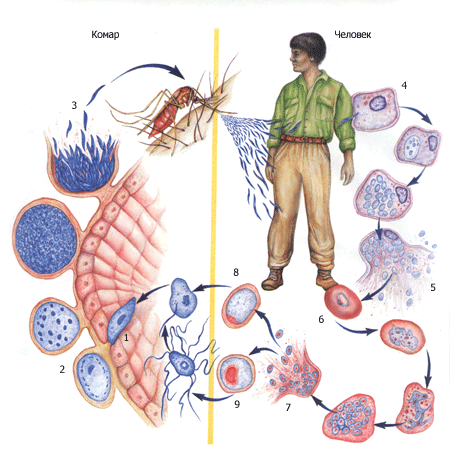
Плазмодий бесполо развивается в человеческих организмах, далее происходит половое развитие в организме самок комаров рода Anopheles. Ребенок заражается, когда его кусает комар, занося со слюной возбудитель. Изначально спорозоиты с кровью попадают в печеночные клетки, где образуются мерозоиты на тканевой фазе развития. Фаза длится около 8 дней при трехдневной малярии, около 6 дней при тропической малярии, 15 дней при четырехдневной. После данной фазы мерозоиты попадают в кровь и эритроциты, начинается эритроцитарная шизогония. В итоге получается разрыв эритроцитов, что приводит к высвобождению подвижных паразитов. Они из плазмы крови вновь внедряются в другие эритроциты, и такой цикл может повторяться 3-4 раза. Далее в крови ребенка появляются женские и мужские половые клетки, которые дальше могут попасть в комариный желудок и там оплодотворяться, что приводит к образованию из гаметоцитов гамет, что называется половым циклом. Конечная форма данного цикла – спорозоиты, которые проникают в гемолимфу комара, а затем в его слюнные железы. Так комар уже опасен для человека с точки зрения возможности заражения малярией.
Диагностика
Обычно установить наличие заболевания можно с помощью общей клинической картины и обнаружения в крови самих паразитов. Чередующиеся лихорадочные приступы, увеличение печени или селезенки, гипохромная анемия может быть следствием болезни, хотя признаки малярии бывают разными. Необходимо уточнить, каким образом могло произойти заражение – определить источник малярии. Если же подозрения подтверждаются, то берут кровь для обследования. При этом при первых приступах лихорадки трудно обнаружить паразитов, поэтому микроскопическое исследование необходимо проводить через несколько суток.
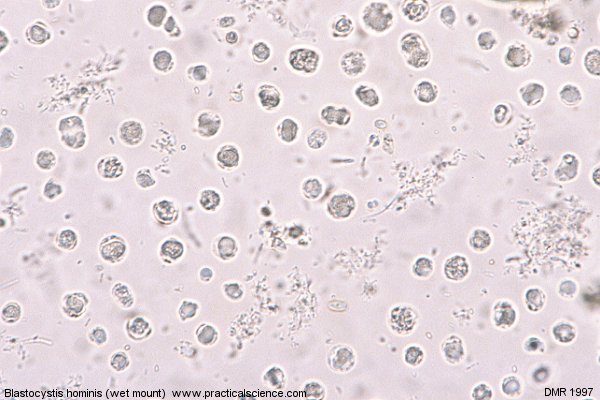
Морфологическая картина простейших при исследовании
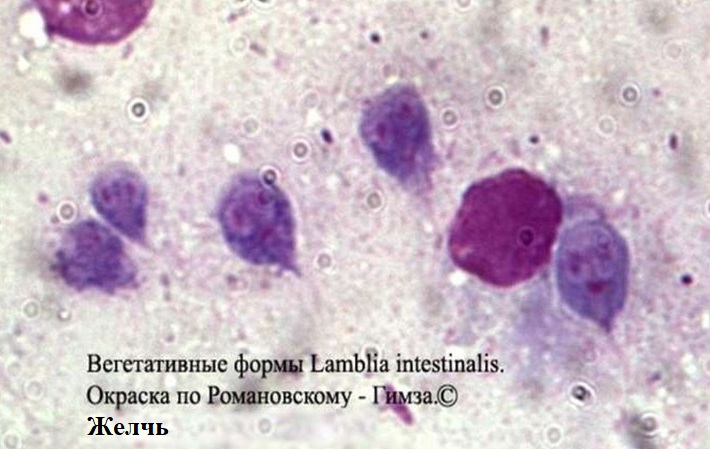
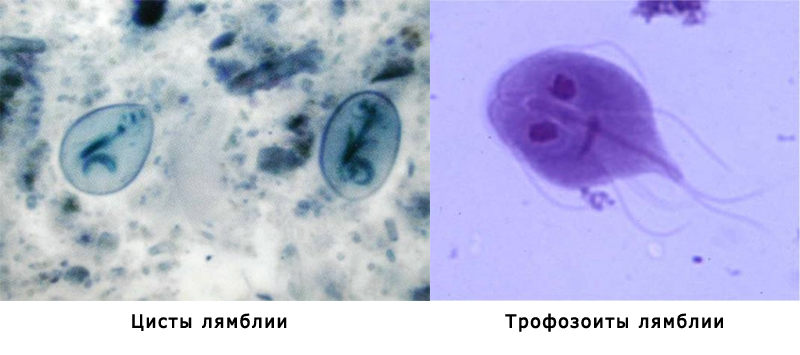
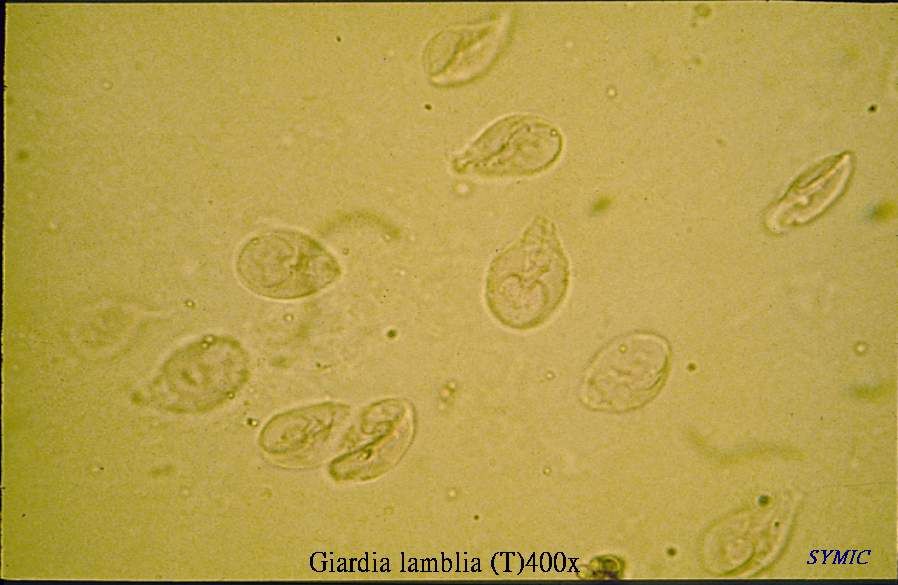
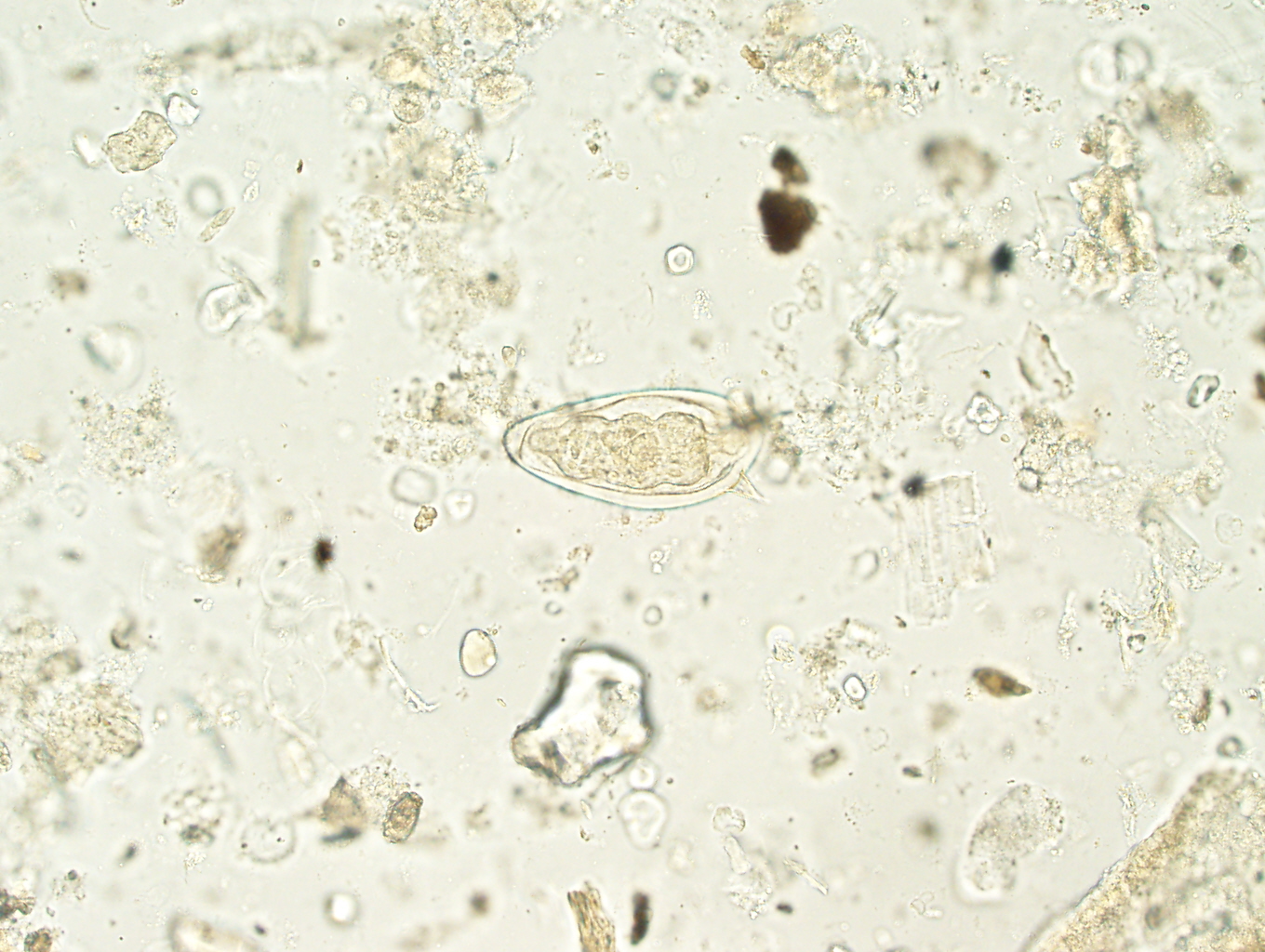
Lamblia intestinalis (лямблии) относится к классу жгутиковых. Лямблии паразитируют в тонкой кишке, преимущественно в двенадцатиперстной кишке, а также в жёлчном пузыре. Существование трофозоитов (вегетативная форма лямблий) требует жидкой среды, поэтому, попадая в толстую кишку, лямблии инцистируются, и в кале обнаруживают только цисты. Лишь при профузной диарее или после действия слабительных в испражнениях удаётся обнаружить вегетативные формы.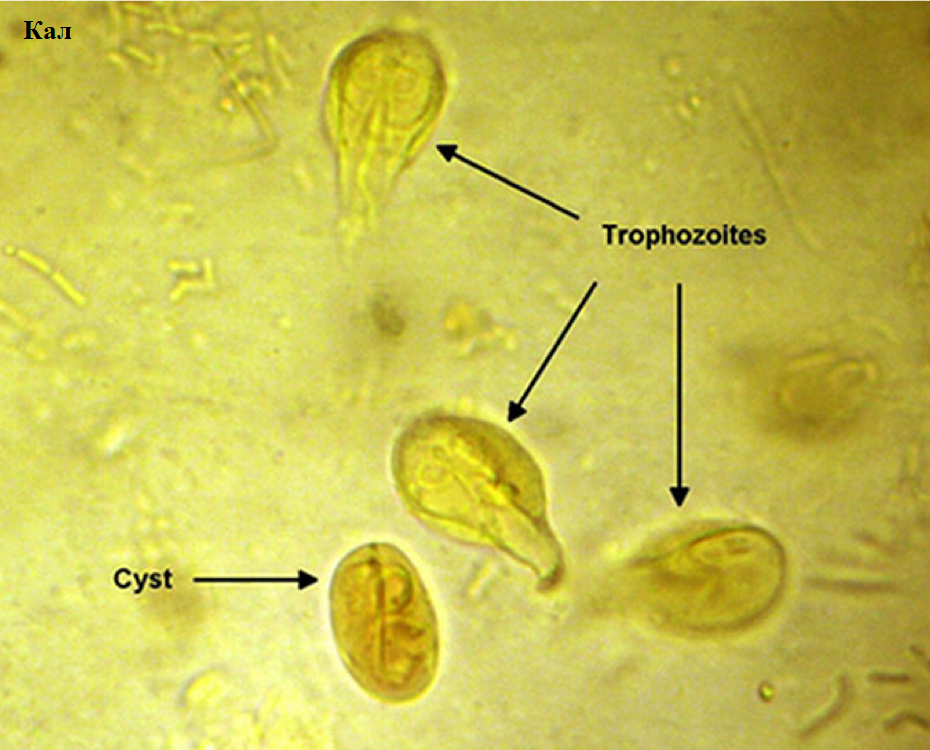
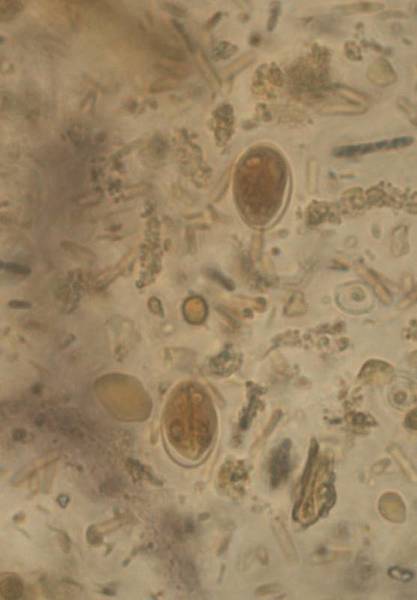
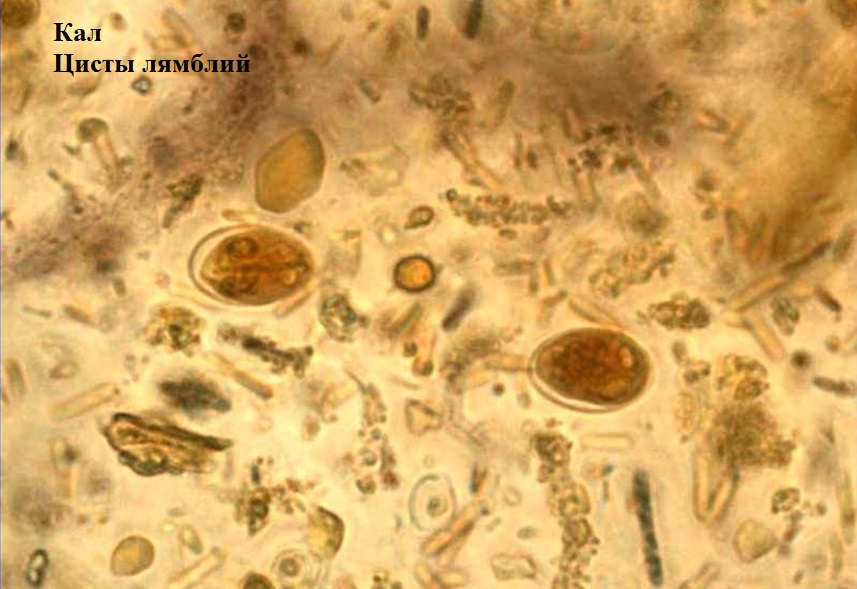
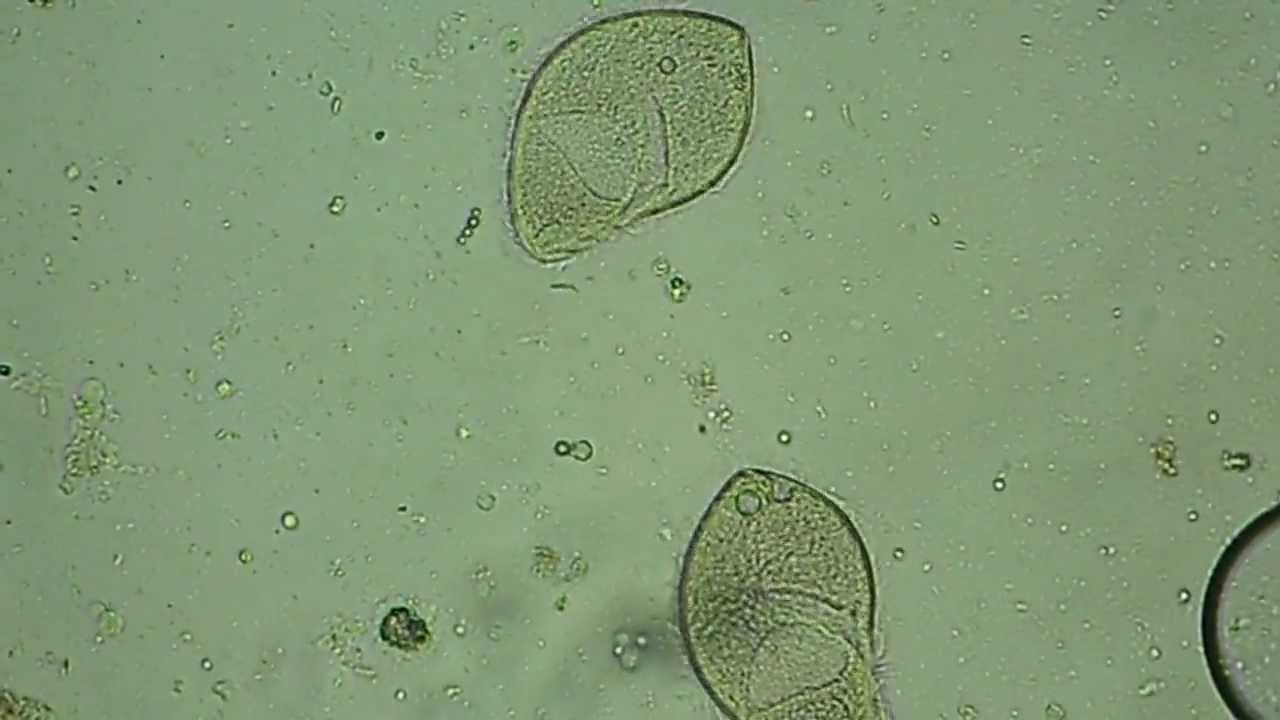
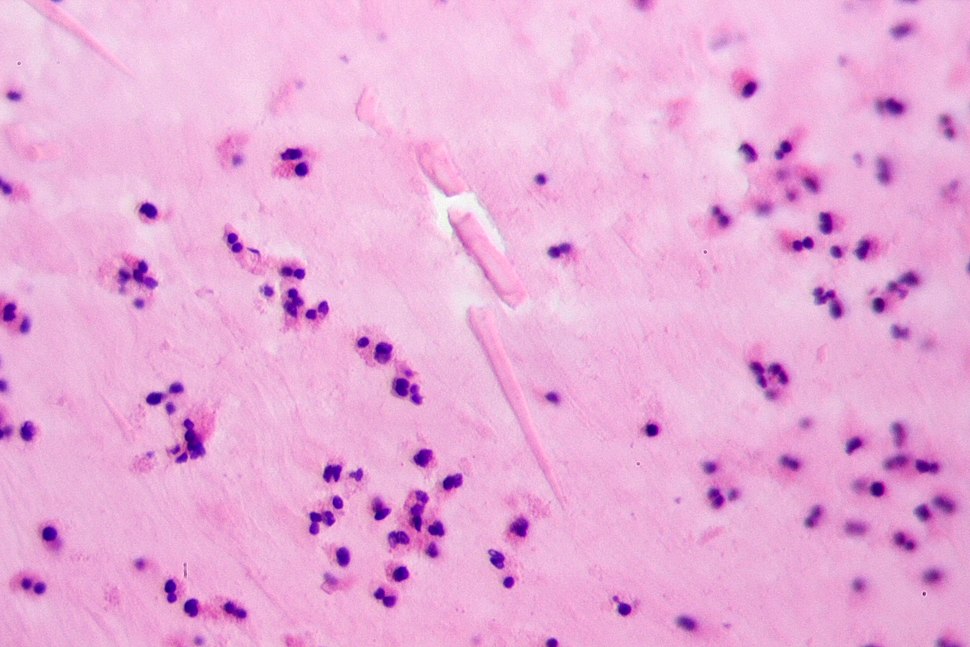
Balantidium coli. Балантидий — единственная ресничная инфузория, паразитирующая в кишечнике человека и вызывающая заболевания различной тяжести — от лёгких колитов до тяжёлых язвенных поражений. Возбудитель обнаруживают в фекалиях в форме трофозоитов или цист. Возможно носительство у здоровых людей. 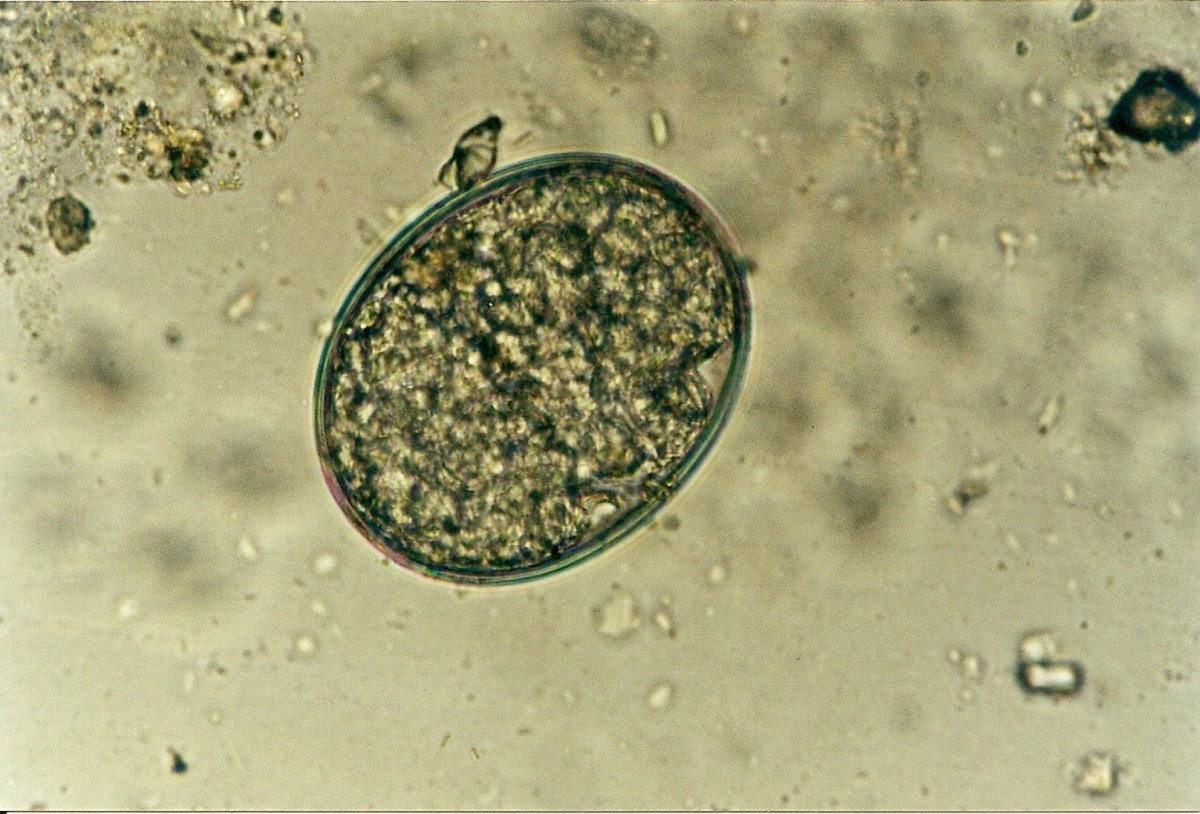
.jpg)
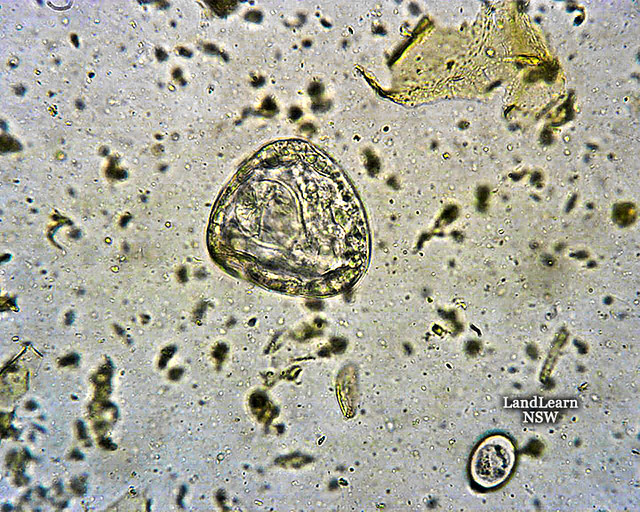
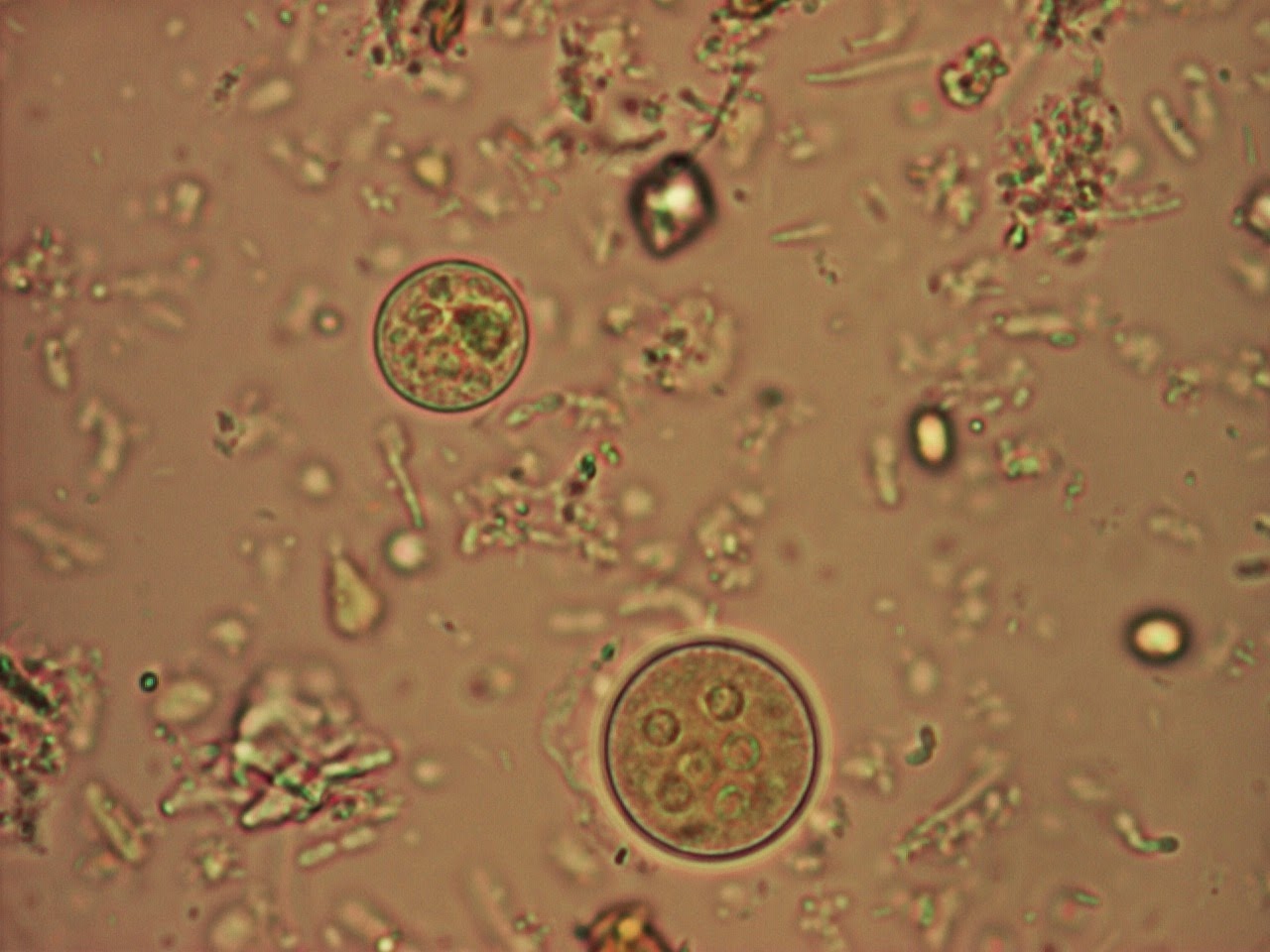
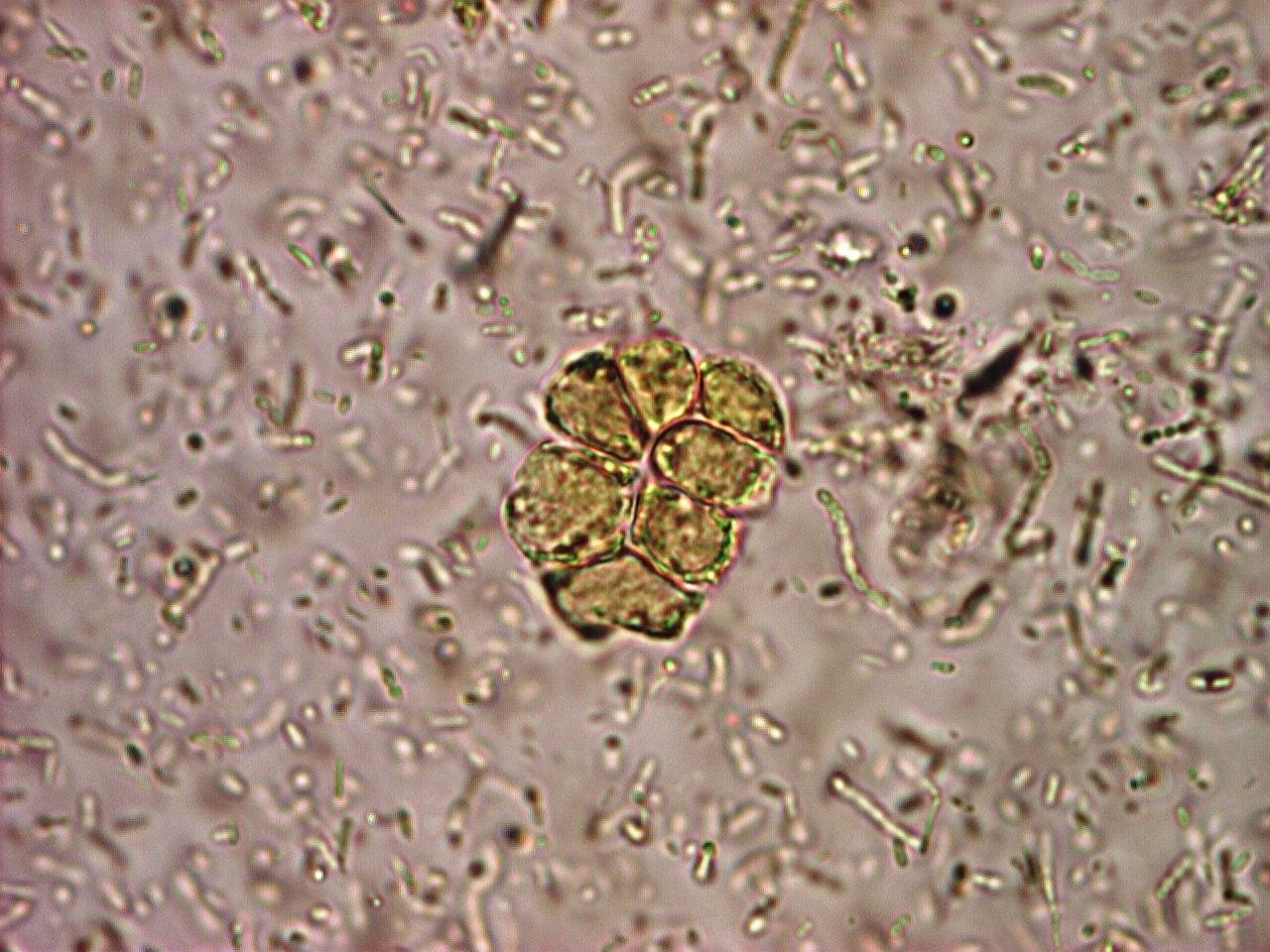
Cryptosporidium. Представителей рода Cryptosporidium в настоящее время рассматривают как важнейших возбудителей диарей. Криптоспоридии (от греч. «скрытая спора») — облигатные паразиты, поражающие микроворсинки слизистых оболочек ЖКТ и дыхательных путей человека и животных. Инфекции ЖКТ, вызванные криптоспоридиями, зарегистрированы во всех странах мира. Такое широкое распространение криптоспоридиоза связано с большим количеством природных резервуаров инфекции, низкой инфицирующей дозой и высокой резистентностью возбудителя к дезинфицирующим веществам и противопаразитарным препаратам.
Среди криптоспоридий потенциально патогенными для человека видами являются Cryptosporidium parvum и Cryptosporidium felis (выявлены у ВИЧ-инфицированных). Наиболее типичная локализация инфекции у человека — дистальные отделы тонкой кишки. У пациентов с выраженными им-мунодефицитами может быть инфицирован весь ЖКТ — от ротоглотки до слизистой оболочки прямой кишки.
Диагностика криптоспоридиоза в большинстве случаев основана на обнаружении ооцист криптоспоридий в испражнениях и/или (значительно реже) в биоптате слизистой оболочки тонкой кишки при синдроме водянистой диареи. Используют микроскопию приготовленных препаратов, окрашенных по Граму. В большинстве случаев данный метод окраски не позволяет выявить ооцисты, вследствие их слабой способности удерживать краситель и невозможности отличить их от дрожжеподобных грибов. Поэтому применяют окраску на кислотоустойчивость. При таком методе окраски ооцисты криптоспоридий окрашиваются в красный или розовый цвет и хорошо видны на сине-фиолетовом фоне, в который окрашиваются другие микроорганизмы и содержимое кишечника.
При остром криптоспоридиозе количество ооцист в фекалиях велико, что позволяет легко их обнаружить при микроскопии окрашенных препаратов. Однако при хроническом криптоспоридиозе с лёгким течением, когда количество ооцист в кале мало, для повышения вероятности их обнаружения необходимо использовать методики обогащения. В последние годы для диагностики криптоспоридиоза стали часто использовать серологические методы.
Криптоспоридиоз желчевыводящих путей может проявляться холециститом, значительно реже гепатитом (с повышением концентрации билирубина, активности АСТ, АЛТ, щелочной фосфатазы в крови) и склеро-зирующим холангитом. Для диагностики билиарного криптоспоридиоза исследуют биоптаты печени и жёлчь, где можно обнаружить криптоспоридии в различных стадиях развития.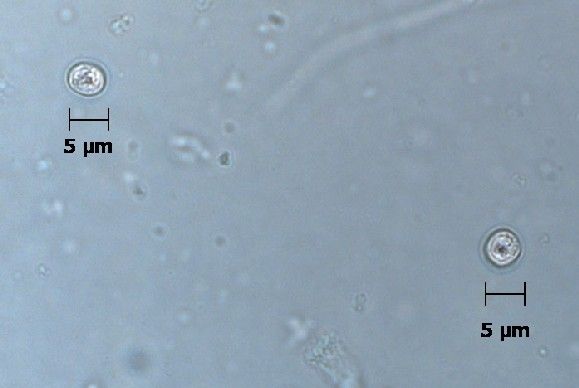
«Дары природы» — человеку
В природе нет ничего лишнего и непродуманного. Человеческий организм — тоже часть природы, поэтому повышение температуры тела не просто неприятные ощущения, от которых мы зачастую стремимся избавиться, принимая лекарства, а сигнал о неполадках в системе и одновременно защитная реакция. Это неспецифический координированный ответ на болезнь.
При вторжении «чужака» (будь то бактерии, вирусы, простейшие или немикробные инородные вещества — антигены) активизируются клетки крови, ответственные за наш иммунитет, – лейкоциты. Эта «армия» защитников состоит из «подразделений», каждое из которых выполняет свою задачу. Лимфоциты, моноциты, нейтрофилы, эозинофилы вступают в борьбу и выделяют особое вещество — лейкоцитарный или эндогенный пироген. При воздействии этого вещества на центр терморегуляции, расположенный в головном мозге, а именно, в переднем гипоталамусе, повышается температура тела. На этом фоне включаются многочисленные механизмы защиты организма: возрастает фагоцитарная активность макрофагов, усиливается продукция интерферонов и антител. Это, так называемый «пирогенный» механизм повышения температуры тела. Вот почему врачи не рекомендуют снижать температуру тела без веских на то оснований.