Аневризма аорты брюшной полости
Содержание:
- Диагностика и лечение
- Методы лечения аневризмы аорты
- Глюкокортикоистероиды в лечении неосложненного ГКА (без поражения органа зрения, аорты и ее ветвей)
- Диагностика
- В переводе с греческого
- Осложнения аневризмы аорты
- Народные средства
- Контроль и лечение
- Лечение ГКА с поражением органа зрения
- Управление
- Лечение
- Факторы риска развития аневризм
- Статистика и факты
- Заключение
Диагностика и лечение
Специальной лабораторной диагностики аневризмы не требуют. Однако с помощью стандартных анализов (общий, биохимический анализы крови) можно заподозрить причину возникновения патологии (при воспалительных процессах будут повышены СОЭ, лейкоциты, С-реактивный белок; при атеросклеротических — соответствующие изменения липидного спектра и повышение общего холестерина).
Инструментальная диагностика аневризмы аорты проводится с помощью:
- Рентгенографии органов грудной клетки;
- Эхокардиографии (УЗИ сердца);
- УЗИ брюшной полости;
- Компьютерной томографии;
- Магнитно-резонансной томографии;
- Рентгеноконтрастной ангиографии (Аортографии);
- Внутрисосудистого ультразвукового исследования (используется крайне редко ввиду малой доступности техники).
Специфическое лечение — только хирургическое — протезирование аорты.
На сегодняшний день в России врачебное сообщество считает необходимым хирургическое лечение рассматривать при наличии аневризмы диаметром от 45-50 мм и при скорости роста аневризмы более 6 мм в год.
Медикаментозную терапию используют для снижения рисков появления осложнений аневризм, то есть их разрывов и для улучшения прогноза после операции. Лечение в таком случае направлено на сопутствующие заболевания: артериальная гипертензия, ишемическая болезнь сердца, болезни легких и почек.
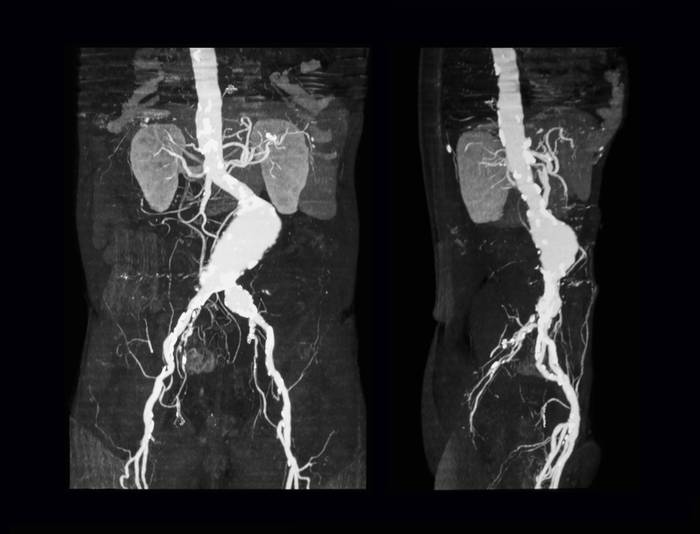
Методы лечения аневризмы аорты
Существует несколько методик лечения аневризмы аорты
Важно знать преимущества и недостатки каждой из этих методик. Подходы к лечению аневризм брюшного отдела аорты:
Наблюдение за пациентом в динамике
При размере аневризмы менее 4,5 см. в диаметре пациенту рекомендовано наблюдение сосудистого хирурга, т. к. риск операции превышает риск разрыва аневризмы аорты. Таким пациентам должны проводится повторные ультразвуковые исследования и/или компьютерная томография не реже 1 раза в 6 месяцев.
При диаметре аневризмы более 5 см. хирургическое вмешательство становится предпочтительным, так как с увеличением размеров аневризмы повышается риск разрыва аневризмы.
Если размер аневризмы увеличивается более чем на 1 см. в год, риск разрыва возрастает и хирургическое лечение также становиться предпочтительным.
Открытое хирургическое вмешательство: резекция аневризмы и протезирование аорты
Хирургическое лечение направлено на профилактику жизнеугрожающих осложнений. Риск хирургического вмешательства связан с возможными осложнениями, которые включают инфаркт, инсульт, потерю конечности, острую ишемию кишечника, сексуальную дисфункцию у мужчин, эмболизацию, инфекцию протеза и почечную недостаточность.
Операция выполняется под общим наркозом. Суть операции в удалении аневризматического расширения и замещение его синтетическим протезом. Средний показатель смертности при открытых вмешательствах составляет 3-5 %. Однако, может быть выше при вовлечении в аневризму почечных и/или подвздошных артерий, а также в силу имеющейся у пациента сопутствующей патологии. Наблюдение в послеоперационном периоде осуществляется один раз в год. Отдаленные результаты лечения хорошие.
Эндоваскулярное протезирование аневризма аорты: установка стент-графта
Эндопротезирование аневризмы аорты является современной альтернативой открытому вмешательству. Операция выполняется под спинальной или местной анестезией через небольшие разрезы/проколы в паховых областях. Через вышеуказанные доступы в бедренную артерию под контролем рентгена вводятся катетеры. По которым, в дальнейшем, будет подводится эндопротез к аневризматическому расширению. Эндопротез или стент-графт брюшной аорты представляет собой сетчатый каркас, выполненный из специального сплава и обернутый синтетическим материалом. Последним этапом операции является установка стент-графта в место аневризматического расширения аорты.
В конечном счете аневризма «выключается» из кровотока и риск ее разрыва становится маловероятным. После эндопротезирования аорты пациент наблюдается в стационаре 2-4 дня и выписывается.
Эта методика позволяет снизить частоту ранних осложнений, сократить сроки пребывания пациентов в стационаре и уменьшить показатель смертности до 1-2%. Наблюдение в послеоперационном периоде осуществляется каждые 4-6 месяцев с использованием ультразвуковых методик, КТ-ангиографии, рентгенконтратной ангиографии. Эндоваскулярный метод лечения, безусловно, менее травматичный. Ежегодно, только в США, проводится около 40 000 подобных операций.
Таким образом, выбор методики лечения аневризмы брюшного аорты основывается на индивидуальных особенностях пациента.
Глюкокортикоистероиды в лечении неосложненного ГКА (без поражения органа зрения, аорты и ее ветвей)
Глюкокортикоиды остаются «золотым стандартом» лечения ГКА. Начальная доза у пациентов с неосложненным ГКА составляет от 0,3 до 1 мг/кг/сут в пересчете на преднизолон. В некоторых исследованиях показано, что дозы 0,5-0,7 мг/кг/сут обычно достаточно для подавления активности болезни, при этом они удовлетворительно переносятся. В рандомизированных клинических исследованиях пульс-терапия метилпреднизолоном (15 мг/кг/сут) до назначения пероральных глюкокортикостероидов обеспечивала дополнительное снижение частоты обострений и оказывала стероидосберегающее действия . Прием препарата в стартовой дозе продолжают в течение 2-4 недель в зависимости от скорости разрешения воспалительных изменений. Снижение дозы глюкокортикоcтероидов начинают быстро, чтобы достичь дозы 15-20 мг/сут за 6-10 недель. Проспективные и ретроспективные исследования показали, что примерно у половины пациентов удается снизить дозу до 7,5-10 мг/сут за 6 месяцев . В то же время прекращение приема глюкокортикостероидов через 6 мес в 77% случаев сопровождалось развитием обострений в течение последующего года . Медиана длительности лечения в когортных исследованиях составляла около 24 мес, однако она варьировалась в широких пределах и иногда достигала нескольких лет.
Диагностика
Диагностика аневризмы аорты часто бывает затруднена из-за отсутствия выраженной симптоматики и схожести признаков патологии с симптомами других заболеваний. При подозрении на аневризму назначается комплекс мероприятий, включающий:
- физикальный осмотр – сбор анамнеза, визуальный осмотр, перкуссия полостей тела, пальпация (при подозрении на брюшную аневризму), прослушивание с помощью фонендоскопа, измерение артериального давления;
- рентгенографию;
- УЗИ;
- МРТ, ЭКГ и КТ.
Важно! Лабораторные анализы при аневризме не информативны, так как патология не вызывает специфических изменений в моче и крови
В переводе с греческого
Диагноз называется аневризма брюшного отдела аорты. Аневризма по гречески – «расширение». Кровь, бегущая по аорте, создает пульсирующее давление на стенки и, если стенки утратили эластичность, они в каких-то местах растягиваются, аорта расширяется, на одной из ее сторон могут образоваться «мешки», которые иногда прорываются. В брюшном отделе аорты это случается гораздо чаще, чем в каком-либо другом.
Причиной аневризмы может быть врожденная слабость соединительной ткани. Влияет на растяжение стенок гипертония, при ней давление в сосудах превышает норму. Осложняет ситуацию атеросклероз, при одном из его видов стенки сосудов деградируют, а сами сосуды расширяются.
Аневризма развивается с возрастом и чаще обнаруживается у людей после 60 лет, в основном у мужчин. Женщины от этого заболевания страдают реже, потому что реже болеют атеросклерозом, их от него защищают гормоны.
Осложнения аневризмы аорты
1. Пороки аортального клапана и сердечная недостаточность. При аневризме восходящей аорты сифилитического происхождения может развиться декомпенсация сердечной деятельности из-за порока аортального клапана или перекрытия устья коронарных артерий.
2. Разрыв аневризмы с кровотечением. Кровотечение может происходить в органы дыхания (бронхи, трахею), плевральную полость, сердечную сумку, в пищевод, крупные кровеносные сосуды, расположенные в грудной полости, и иногда даже наружу через кожу при разрушении грудины. В случае кровотечения в полость перикарда возникает тампонада сердца. Кровотечение приводит к быстро нарастающей кровопотере.
3. Острое и подострое тромбирование аневризмы аорты. Чаще всего развивается в брюшном отделе аорты и приводит к закрытию расположенных здесь её ветвей.
Перечисленные осложнения быстро ведуг к гибели пациента, если вовремя не приняты соответствующие меры.
Народные средства
Аневризму аорты нельзя вылечить консервативными методами, в том числе – народными средствами. Единственным способом радикального лечения патологии является хирургическое вмешательство. При наличии противопоказаний к операции или выборе выжидательной тактики лечения больным назначают традиционные аптечные препараты, которые нельзя заменять народными рецептами. Самолечение при данной патологии может представлять угрозу для жизни и здоровья больного.
Информация носит справочный характер и не является руководством к действию. Не занимайтесь самолечением. При первых симптомах заболевания .
Контроль и лечение
- аневризмы часто протекают бессимптомно;
- аневризмы брюшной аорты часто обнаруживаются случайно при обследовании живота при выполнении рентгенографии, компьютерной томографии, УЗИ, выполненных с другой целью;
- если аневризма маленькая (4.5 см в диаметре) и никаких симптомов нет, рекомендуется ежегодное дуплексное ультразвуковое обследование;
- отказ от курения и контроль гипертонии – оптимальная профилактика появления и роста аневризм;
- оперировать рекомендуется аневризмы с диаметром больше 5 см у женщинах и 5.5 см у мужчин, или если аневризма увеличилась на 5 мм (или больше) меньше чем за 6 месяцев.
Процедура проводится через небольшие разрезы в бедренных артериях. После пункции бедренной артерии проводник проводится через расширенную часть аорты, затем стент продвигается по проводнику. После правильного расположения стента, баллон расширяется, и стент раздвигает стенку сосуда, чтобы не допустить распространения аневризмы ниже почечных артерий.
Для гарантии надлежащей герметизации между имплантируемым стентом и аортой, большинство в настоящее время доступных стентов требует, чтобы у аневризмы проксимальный перешеек был по крайней мере на 1.0 — 1.5 см ниже почечных артерий. Однако, операция может быть сделана пациентам с аневризмами, у которых перешейки аневризмы короче или вообще отсутствуют, при помощи имплантации стента с многочисленными отверстиями и браншами к артериям почек или кишечника.
Для проведения проводника требуется подходящее состояние подвздошных артерий, однако возможное введение стента через маленький забрюшинный разрез увеличило число кандидатов на эндоваскулярную операцию
По сравнению с традиционным открытым хирургическим вмешательством эндоваскулярное имеет несколько преимуществ:
- уменьшение времени операции;
- уменьшение кровопотери и необходимости инфузий;
- уменьшение времени лечения в отделении интенсивной терапии и пребывания в больнице;
- уменьшенный риск осложнений;
- используется меньше контраста, и часто во время процедуры требуется меньше 60 мл контраста;
- интраоперационная и ранняя (до 30 дней) смертность также меньше для эндоваскулярных операций, чем для открытых.
В среднем пребывание после открытой операции в отделении интенсивной терапии составляет приблизительно 3 дня, затем 7-10 дней в отделении, восстановление занимает 8-12 недель.
Большинство пациентов после эндоваскулярной операции не требуют госпитализации в отделение ИТ и могут быть отпущены домой на следующий день после операции. Больший процент пациентов, перенесший эндоваскулярную операцию, отпускаются сразу домой, а не в реабилитационные санатории. Эти пациенты быстрее возвращаются к нормальному уровню физической активности, реабилитационный период составляет 1-2 недели.
У пациентов с незначительной сопутствующей патологией, которым возможно провести эндоваскулярное вмешательство, также могут произойти некоторые осложнения, специфичные для этого метода. Крайне редко возможен переход к открытой операции. Проблемы, связанные с установкой стента, возникают у 5-10% пациентов и требуют КТ или УЗИ наблюдения
Смещение стента возможно редко, т.к. у стентов нового поколения имеются крючки, и они раскрываются выше уровня почечных артерий для лучшей фиксации. «Подтекания» — когда кровь проникает между стентом и стенкой аорты – встречается в 5-10% случаев. Большая их часть – II типа «подтекания» — кровь продолжается скапливается в аневризме из поясничной артерии. Если есть рост аневризмы, пациенты не считаются излеченными, в этом случае под местной анестезией амбулаторно проводят закрытие поясничных артерий эмболизацией.
При надлежащем наблюдении риск последующего разрыва чрезвычайно низок. Поэтому пациенты должны быть готовы выполнять в дальнейшем обследование, которое включает компьютерную томографию эндоваскулярного стента спустя 4 — 6 месяцев после операции и затем ежегодно. Другие менее распространенные осложнения – разрушение или инфицирование стента.
Современный прогноз для здоровых пациентов, которые переносят операцию на аневризме, превосходен. Эндоваскулярная операция является удивительным прогрессом в лечении пациентов с подходящей анатомией и является преимущественным методом лечения пациентов с высокой степенью риска и пожилых.
Лечение ГКА с поражением органа зрения
Поражение органа зрения – наиболее частое тяжелое осложнение ГКА, которое в 13-19% случаев приводит к необратимому снижению остроты зрения или слепоте вследствие окклюзии ветвей зрительной артерии или, реже, инсульта в бассейне задней затылочной артерии. В трети случаев отмечается поражение обоих глаз. У 95% пациентов нарушение зрения развивается до начала лечения глюкокортикоидами, а у 20% больных представляет собой первое проявление васкулита. У небольшой части больных терапия глюкокортикостероидами, начатая в течение первых 72 ч после ухудшения зрения, позволяет добиться частичного его восстановления. Лучших результатов удавалось добиться при назначении преднизолона внутрь в дозе как минимум 60 мг/сут или метилпреднизолона в дозе 500 мг внутривенно . По данным двух ретроспективных исследований высказано предположение, что низкие дозы аспирина позволяют предотвратить ишемические поражения органа зрения и центральной нервной системы , хотя этот вопрос остается спорным, учитывая отсутствие адекватных исследований.
Управление
Варианты лечения бессимптомной АБА — консервативное ведение, наблюдение с целью возможного выздоровления и немедленное лечение . Доступны два режима лечения АБА: открытая пластика аневризмы и эндоваскулярная пластика аневризмы ( EVAR ). Вмешательство часто рекомендуется, если аневризма разрастается более чем на 1 см в год или превышает 5,5 см. Ремонт также показан при симптоматических аневризмах. Через десять лет после открытого восстановления AAA общая выживаемость составила 59%.
Консервативный
Консервативное лечение показано людям, у которых восстановление сопряжено с высоким риском смерти, и пациентам, у которых восстановление вряд ли приведет к увеличению продолжительности жизни. Основа консервативного лечения — отказ от курения .
Наблюдение показано при небольших бессимптомных аневризмах (менее 5,5 см), когда риск заживления превышает риск разрыва. По мере увеличения диаметра AAA увеличивается риск разрыва. Наблюдение до тех пор, пока диаметр аневризмы не достигнет 5,5 см, не имеет более высокого риска по сравнению с ранним вмешательством.
Медикамент
Не было обнаружено, что медикаментозное лечение эффективно снижает скорость роста или частоту разрыва бессимптомных АБК. Тем не менее, лечение артериального давления и липидов следует проводить в обычном режиме.
Операция
Порог для ремонта незначительно варьируется от человека к человеку, в зависимости от баланса рисков и преимуществ при рассмотрении вопроса о ремонте по сравнению с постоянным наблюдением. На это может влиять размер собственной аорты человека, а также наличие сопутствующих заболеваний, которые увеличивают операционный риск или сокращают продолжительность жизни. Однако доказательства обычно не подтверждают ремонт, если размер меньше 5,5 см.
Открытый ремонт
Открытая пластика показана молодым пациентам в качестве плановой процедуры, а также при растущих или больших, симптоматических или разорванных аневризмах. Во время операции необходимо перерезать аорту, не допуская попадания крови в органы брюшной полости и отделы спинного мозга ; это может вызвать ряд осложнений
Важно, чтобы критическая часть операции была быстрой, поэтому разрез обычно делают достаточно большим, чтобы облегчить скорейшее восстановление. Восстановление после открытой операции на АБА требует значительного времени
Минимум — несколько дней в отделении интенсивной терапии, всего неделя в больнице и несколько месяцев до полного выздоровления.
Эндоваскулярное восстановление
Эндопротез брюшной аорты, компьютерная томография, исходная аневризма отмечена синим цветом
Эндоваскулярная пластика впервые стала применяться в 1990-х годах, и, хотя в настоящее время она является признанной альтернативой открытой пластике, ее роль еще предстоит четко определить. Обычно он показан пожилым пациентам из группы высокого риска или пациентам, не пригодным для открытого восстановления. Однако эндоваскулярное восстановление возможно только для части AAA, в зависимости от морфологии аневризмы. Основные преимущества перед открытой пластикой заключаются в меньшей периоперационной смертности, меньшем времени в отделении интенсивной терапии , меньшем времени в больнице в целом и более раннем возвращении к нормальной деятельности. Недостатки эндоваскулярного восстановления включают необходимость более частых текущих осмотров в больнице и более высокую вероятность того, что потребуются дальнейшие процедуры. Согласно последним исследованиям, процедура EVAR не дает никаких преимуществ для общей выживаемости или качества жизни, связанного со здоровьем, по сравнению с открытой операцией, хотя смертность от аневризмы ниже. У пациентов, непригодных к открытой пластике, EVAR плюс консервативное лечение ассоциировалось с отсутствием пользы, большим количеством осложнений, последующими процедурами и более высокими затратами по сравнению с одним консервативным лечением. Также возможно эндоваскулярное лечение параанастомотических аневризм после реконструкции аортобрюзги. В Кокрановском обзоре 2017 г. были обнаружены предварительные доказательства отсутствия разницы в результатах между эндоваскулярным и открытым лечением разрыва АБА в течение первого месяца.
У пациентов с разрывом аорты AAA лечение представляет собой немедленное хирургическое вмешательство. По-видимому, есть преимущества в разрешении разрешающей гипотензии и ограничении использования внутривенных жидкостей во время транспортировки в операционную.
Лечение
Лечение асцита у онкологических больных имеет некоторые особенности
Во-первых, первопричиной скопления жидкости в животе у таких больных является рак, поэтому важно проводить противоопухолевую терапию. Во-вторых, консервативные меры, такие как специальная диета, ограничение соли и мочегонные препараты в данном случае сами по себе неэффективны
Они применяются лишь как дополнение к основному лечению.
Онкологические больные со скоплением жидкости в брюшной полости — это, как правило, пациенты с поздней стадией рака. Асцит существенно ухудшает прогноз, снижает показатели выживаемости. Тем не менее, своевременное паллиативное лечение помогает улучшить состояние больного и продлить его жизнь.
Лапароцентез и дренирование брюшной полости
Первой мерой помощи онкологическим пациентам с асцитом является лапароцентез, или парацентез. Во время этой процедуры в брюшной стенке с помощью специального инструмента под контролем УЗИ делают прокол и выводят лишнюю жидкость. Лапароцентез проводят под местной анестезией, и после него состояние пациента обычно существенно улучшается: перестает беспокоить дискомфорт в животе, тошнота, рвота, одышка. Если приходится удалять много жидкости, проводят инфузионную терапию, чтобы восполнить потери жидкости и белка. Считается, что можно безопасно удалять до 4 литров асцитической жидкости в день.
Но со временем жидкость в брюшной полости накапливается снова. Для ее постоянного оттока устанавливают перитонеальный катетер: трубку, по которой жидкость постоянно оттекает в подсоединенный резервуар. В современных клиниках для этого также применяют перитонеальные порт-системы. Такое устройство представляет собой небольшой резервуар из титана, одна из стенок которого выполнена в виде специальной мембраны. Его подшивают под кожу и соединяют катетером с брюшной полостью. Это позволяет повторно выводить жидкость, не делая новых проколов в брюшной стенке.
Проводят интраперитонеальную химиотерапию — введение химиопрепаратов непосредственно в брюшную полость через перитонеальный катетер или порт-систему. Лекарство уничтожает опухолевые клетки, распространяющиеся по поверхности брюшины, за счет чего уменьшается накопление жидкости.
Хирургические методики
В некоторых случаях для борьбы с асцитом прибегают к хирургическим вмешательствам. Например, может быть выполнено портокавальное шунтирование — наложение анастомозов (сообщений) между системами полой и воротной вен, чтобы снизить давление в последней.
Иногда проводят частичную деперитонезацию — удаляют часть брюшины, покрывающей стенки брюшной полости. Также практикуется оментогепатофренопексия — подшивание сальника к печени и диафрагме, это помогает улучшить отток жидкости.
Скопление жидкости в брюшной полости у онкобольных — опасное осложнение, борьбу с ним нужно начинать как можно быстрее. В Международной клинике Медика24 пациента готовы принять в любое время суток. Наши врачи оперативно проведут обследование в необходимом объеме, окажут помощь и спланируют дальнейшую тактику лечения в соответствии с современными международными рекомендациями. У нас проводятся все виды лечения онкологических заболеваний, наши врачи имеют большой опыт в лечении злокачественного асцита.
Материал подготовлен врачом-онкологом, торако-абдоминальным хирургом Международной клиники Медика24 Коротаевым Александром Валерьевичем.
Факторы риска развития аневризм
К развитию аневризм предрасполагает потеря эластичности и прочности стенки сосуда. Слабость сосудистой стенки может быть обусловлена врожденными особенностями или воздействием внешних факторов. Основные причины развития болезни:
- атеросклероз ー образование холестериновых бляшек;
- воспаление стенки аорты (бывает при травматическом повреждении, сифилисе, грибковом поражении);
- аутоиммунные заболевания;
- врожденные патологии соединительной ткани (муковисцидоз, синдром Марфана);
- травматизация при выполнении диагностических и лечебных манипуляций (коронарография, операции на сердце).
Статистика и факты
Аневризма брюшной аорты (АБА) это локальное или диффузное расширение диаметра аорты более чем 2 раза. Аневризма брюшной аорты составляют 95% от всех аневризм, при этом примерно у 9% людей старше 65 лет заболевание протекает бессимптомно. Частота заболевания составляет 2-5% среди мужчин старше 60 лет. Пик заболеваемости у мужчин отмечается после 80 лет, а у женщин после 90 лет, соотношение мужчин и женщин с АБА 4:1.
К сожалению, течение заболевания прогрессирующее. Размер аневризмы увеличивается в среднем на 10% в год, часто без симптомов и единственным проявлением заболевания может быть ее разрыв со смертельным исходом. Ежегодно в мире диагностируется до 200 000 случаев аневризм брюшной аорты.
В США от разрывов и послеоперационных осложнений АБА умирает до 15 000 человек в год, при этом от 30 до 50% пациентов погибает от разрыва аневризм брюшной аорты до оказания медицинской помощи. Аневризма брюшной аорты занимает 15-е место среди всех причин смерти и 10-е место среди причин смерти у мужчин старше 60 лет.
Существует несколько классификаций аневризм брюшной аорты. Наибольшее распространение получила анатомическая классификация, согласно которой различают аневризмы расположенные ниже почечных артерий — инфраренальные (95% АБА) и выше почечных артерий — супраренальные.
Примерно в четверти случаев АБА – в процесс вовлечены и подвздошные артерии (артерии таза, которые отходят от брюшной аорты). В 12 % случаев АБА сочетается с аневризмой выше расположенной грудной части аорты. Основные факторы риска возникновения аневризмы это: мужской пол (5-6-кратный риск), возраст (1.7-кратный риск).
Наличие аневризмы у членов семьи увеличивает риск развития АБА в двое. Так, например, от 15 до 25 % пациентов с АБА имеют или имели родственника первой степени с аневризмой брюшной аорты.
Важным фактором возникновения и развития аневризмы брюшной аорты является курение. Так курильщиков с АБА в пять раз больше чем некурящих, 75% пациентов с АБА 4 см и более – курильщики. Риск возникновения аневризмы брюшной аорты увеличивается в зависимости от стажа курения и ежедневного количества выкуриваемых сигарет.
Риск разрыва аневризмы увеличивается при артериальной гипертонии, наличии хронических заболеваний легких, определенных формах аневризматического мешка (симметричные аневризмы меньше подвержены разрыву, чем ассиметричные). Однако основной фактор разрыва – размер аневризматического мешка.
Смертность при аневризме брюшной аорты с диаметром 4 см менее 5% в год, а смертность при АБА в с внутренним диаметром более 9 см составляет более 75 % в год.
Заключение
Диагноз ГКА, развивающегося у людей пожилого и старческого возраста, нередко устанавливают с опозданием, что может привести к тяжелым последствиям, в частности потере зрения
В связи с этим французские рекомендации по диагностике и лечению этого заболевания имеют важное значение для врачей различных специальностей, в том числе ревматологов, терапевтов, офтальмологов и неврологов. Следует отметить, что подходы к диагностике и лечению ГКА постепенно меняются
Сегодня многие эксперты признают возможность использования ультразвукового сканирования и других неинвазивных визуализирующих методов как альтернативы биопсии височной артерии, которая в нашей стране проводится значительно реже, чем в зарубежных клиниках. Например, в исследовании GiACTA признаки васкулита крупной артерии, выявленные при ангиографии, КТ- или МР-ангиографии или ПЭТ/КТ, служили самостоятельным критерием диагноза ГКА (т.е. в этом случае не требовалось его подтверждение при гистологическом исследовании). Возможный алгоритм диагностики ГКА, разработанный на основе исследования GiACTA и мнения авторов данной статьи, приведен на рис. 2. Основой лечения ГКА остаются глюкокортикостероиды, однако с учетом результатов исследования GiACTA можно ожидать расширения показаний к назначению тоцилизумаба пациентам с этим системным васкулитом (тяжелое или рецидивирующее течение, серьезные осложения, например, потеря зрения, сохранение активности несмотря на лечение глюкокортикостероидами, осложнения глюкокортикостероидной терапии, требующие применения стероидосберегающих препаратов).