Болезнь паркинсона
Содержание:
Этиология болезни Паркинсона
Физиология нервной системы.
Все движения человека контролируются центральной нервной системой, в которую входят головной и спинной мозг. Стоит человеку лишь подумать о каком-либо намеренном движении, кора головного мозга уже приводит в готовность все отделы нервной системы, ответственные за это движение. Одним из таких отделов являются так называемые базальные ганглии. Это вспомогательная двигательная система, отвечающая за то, как быстро осуществляется движение, а также за точность и качество этих движений.

Информация о движении поступает из коры головного мозга в базальные ганглии, которые определяют, какие мышцы будут в нем участвовать, и насколько каждая из мышц должна быть напряжена, чтобы движения были максимально точными и целенаправленными.
Базальные ганглии передают свои импульсы с помощью специальных химических соединений – нейромедиаторов. От их количества и механизма действия (возбуждающий или тормозящий) зависит, как будут работать мышцы. Основным нейромедиатором является дофамин, который тормозит избыток импульсов, и тем самым контролирует точность движений и степень сокращения мышц.
Чёрная субстанция (Substantia nigra) участвует в сложной координации движений, поставляя дофамин полосатому телу и передавая сигналы от базальных ганглиев к другим структурам мозга. Черная субстанция потому так и названа, что эта зона мозга имеет темную окраску: нейроны там содержат некоторое количество меланина — побочного продукта синтеза дофамина. Именно недостаточность дофамина в черной субстанции мозга приводит к болезни Паркинсона.

Болезнь Паркинсона – что это такое
Болезнь Паркинсона – это нейродегенеративное заболевание головного мозга, которое у большинства пациентов прогрессирует медленно. Симптомы недуга могут постепенно проявляться в течение нескольких лет.
Заболевание возникает на фоне гибели большого количества нейронов в определённых участках базальных ганглиев и разрушение нервных волокон. Для того, чтобы симптомы болезни Паркинсона начали проявляться, должны утратить свою функцию порядка 80% нейронов. В таком случае она неизлечима и прогрессирует с годами, даже несмотря на предпринимаемое лечение.
Также характерным признаком этого заболевания является снижение количества дофамина. Его становится недостаточно для торможения постоянных возбуждающих сигналов коры головного мозга. Импульсы получают возможность проходить прямо до мышц и стимулировать их сокращение. Этим объясняются основные симптомы болезни Паркинсона: постоянные мышечные сокращения (тремор, дрожание), скованность мышц из-за чрезмерно увеличенного тонуса (ригидность), нарушение произвольных движений тела.
Паркинсонизм и болезнь Паркинсона, отличия
Различают:
- первичный паркинсонизм или болезнь Паркинсона, он встречается чаще и носит необратимый характер;
- вторичный паркинсонизм – эта патология обусловлена инфекционными, травматическими и другими поражениями мозга, как правило, носит обратимый характер.
- Спровоцировать болезнь в этом случае может:
- энцефалит;
- травмы головного мозга;
- отравления токсическими веществами;
- сосудистые заболевания, в частности, атеросклероз, инсульт, ишемическая атака и др.
Симптомы
Классическим признаком болезни Паркинсона считают тремор – дрожание конечностей, головы. Однако зачастую именно этот симптом, который, безусловно, имеет место быть, считают ведущим и едва ли не единственным, что приводит многих людей к панике, при появлении дрожи в руках или голове. Однако это не так.
Главным и обязательным симптомом заболевания является олигобрадикинезия – недостаточный объем движений, их скудность, трудность начала движения. Также олигобрадикинезия приводит к скудности мимики, жестов. И лишь при наличии данного симптома может идти речь о болезни Паркинсона
Два других типичных и частых проявления – тремор и ригидность (скованность мышц вследствие повышения их тонуса) зачастую встречаются при других заболеваниях, однако имеют также важное диагностическое значение
Также при болезни Паркинсона могут отмечаться нарушения со стороны двигательной сферы, например, постуральная неустойчивость или невозможность самостоятельно прекратить движение, приводящее к падению. Именно этот симптом зачастую становится инвалидизирующим на поздних стадиях заболевания.
Часто при болезни Паркинсона встречаются когнитивные нарушения (нарушения памяти, концентрации внимания, способности к обучению), тазовые нарушения (чаще запоры), психические нарушения. В большинство случаев болезнь, особенно на поздних стадиях приводит к глубокому психотравмирующему воздействию на больного (а зачастую и на родственников) и приводит к развитию клинически или субклинически выраженной депрессии. Это также надо учитывать, ведь под маской депрессии можно не заметить многие проблемы у больного: он просто о них не самостоятельно скажет.
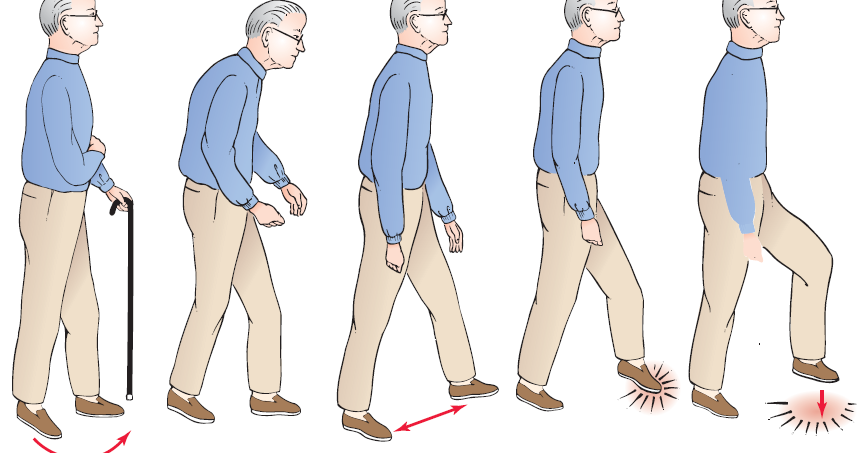
Нередко больные изменяются в поведении (становятся педантичными, непоследовательными, излишне навязчивыми, развивается стойко сниженный фон настроения). У больных также нарушается качество и режим сна. Также являются характерными типичная поза (поза просителя), нарушения походки (походка маленькими шажками) и многие другие признаки.
Если же брать наиболее «популярный» и известный симптом – тремор – то у него имеются свои особенности. Для тремора при болезни Паркинсона характерно одностороннее начало, чаще в руке, с постепенным переходом на другую сторону, а далее на другую анатомическую зону (ноги и т.д.). Тремор челюсти, головы менее характерен и обычно имеет место при поздних стадиях заболевания, да и тогда лишь в редких случаях. Также обращает на себя и сам вид тремора, он напоминает «счет монет» или перебирание таблеток. Тремор обычно малоамплитудный, несколько уменьшается в процессе совершения целенаправленного движения, что особенно ярко заметно при проведении пальце-носовой пробы, во время движения пальца дрожи почти нет, тогда как при завершении целенаправленного действия (попадание в нос) появляется четко различимый тремор.
Известные люди с болезнью Паркинсона.
Стадии
Для определения тяжести состояния болезнь Паркинсона принято разделять на несколько периодов – стадий
Понимание стадии важно для правильного выбора методики лечения
- 1 стадия. Нарушения двигательной активности одной из рук, бессонница, проблемы с обаянием. Позже появляется тремор, существенно ухудшается почерк, ощущается скованность в верхней части спины, иногда – в области шеи.
- 2 стадия. Нарушения двигательной функции заметны с обеих сторон. Дрожать начинает нижняя челюсть и язык, может замедлиться речь, исказиться мимика лица. У многих появляются проблемы с потоотделением (характерный признак – влажные или, напротив, чрезмерно сухие ладони).
- 3 стадия. Изменяется походка. При ходьбе человек начинает непроизвольно ставить ступни параллельно друг другу. Сами шаги становятся семенящими, мелкими. Начинает формироваться так называемая «поза просителя»: полусогнутые ноги + согнутая голова + сутулая осанка. Человек ещё способен обслужить себя, но многие вещи в быту становятся для него очень трудными в выполнении.
- 4 стадия. Полная потеря равновесия. Упасть вперёд человек может даже, вставая с постели. Речь становится невнятной, смазанной, голос – тихим. Настроение – чрезмерно подавленное. Для совершения элементарных дел (например, чистка зубов) требуется помощь близких.
- 5 стадия. Больной не может ходить, самостоятельно садиться. Процесс мочеиспускания становится неконтролируемым. Возникают серьёзные нарушения глотания. Речь похожа на лепет ребёнка.
Излечима ли болезнь?
В наше время врачи смогли разработать эффективные медикаментозные методики симптоматического лечения. К сожалению, медикаментозная терапия не помогает победить причину патологии, но существенно облегчает проявление заболевания, уменьшают осложнения, увеличивает продолжительность жизни пациентов.
Если болезнь развивается в возрасте 40-65 лет, то пациенты живут ещё около 20 лет. Если настигла в более раннем возрасте, то прогнозируемая продолжительность жизни – ещё около 40 лет.
Главное, важно своевременно провести комплексную диагностику и начать лечение под контролем опытного невролога, нейрохирурга. Некоторые пациенты, страдающие даже 3-ей стадией заболевания, своевременно начав лечение, возвращаются на работу, требующую двигательной, интеллектуальной активности
Лучше всего взять болезнь под контроль получается взять при использовании нейрохирургических методик или комбинировании медикаментозного лечения с физиотерапией – особенно гипобарической оксигинацией (процедурами в барокамере), массажем.
Медикаментозное лечение
Современное медикаментозное лечение базируется на использовании препаратов нескольких групп:
- Блокаторы моноаминооксидазы-Б и катехол-О-метилтрансферазы. Благодаря ним создаются препятствия для разрушения гормона дофамина.
- Активаторы (стимуляторы) рецепторов к дофамину.
- Лекарства, которые подавляют действия периферической декарбоксилазы L-аминокислот (ингибиторы).
- Блокаторы действия холина и его аналогов (такими лекарствами можно влиять непосредственно на механизм передачи нервных импульсов).
- Амантадины – препараты, которые увеличивают чувствительность ряда рецепторов.
Выбор того, как лечить болезнь Паркинсона, зависит от стадии заболевания. Если на 1-й стадии болезни акцент делается на стимуляторы рецепторов к дофамину, то на 5-й стадии лечение – максимально комплексное, и нельзя обойтись без ингибиторов периферической декарбоксилазы.
Хирургическое лечение
С 50-х годов 20-го века при лечении болезни Паркинсона используется и хирургическое вмешательство. При этом методики нейрохирургов претерпели существенные изменения. Первоначально операции были направлены на разрушение проводящих путей в таламусе. Увы, результат таких операций часто был неудовлетворительным, а вот побочных действий было очень много.
Более прогрессивный метод – нейропротезирование (нейроимплантация) или установка нейростимуляторов. Человеку ставятся специальные имплантаты. Они активизируют нервные клетки в мозге, улучшают способность мозга обрабатывать информацию, управлять движениями.
После операции может потребоваться дальнейшее медикаментозное поддерживающее лечение, но количество препаратов, требующихся пациенту, существенно сокращается. Уже сразу после операции существенно уменьшается дрожь, улучшается равновесие, способность концентрироваться.
Классификация заболевания
Болезнь Паркинсона является той патологией, которую врачи могут идентифицировать у пациентов во всем мире. Заболевание можно классифицировать по множеству критериев – возрасту, когда первые признаки болезни начали проявляться, проявлениям, стадиям протекания и прочему. Знание основ классификации паркинсонизма помогает выработать правильную тактику лечения заболевания на ранних стадиях.
По возрасту начала болезни
Болезнью Паркинсона страдают многие пожилые люди, после 65 лет данный диагноз слышит 1% всего населения планеты, а после 85 – более 2,5% людей. В среднем, заболевание начинается у пациентов после 55 лет, но бывают случаи паркинсонизма с ранним началом – в 10% всех известных науке случаев заболевание возникло в возрасте до 40 лет, либо даже в возрасте до 20 лет, что свидетельствует о ювенильном паркинсонизме.
Под ювенильным паркинсонизмом следует понимать ранний генетически детерминированный паркинсонизм, возникающий в возрасте до 20-25 лет. Проявляется клиника такой патологии симметричными статическими и кинетическими дрожаниями, дискинезией, пирамидными знаками, интеллектуальной сохранностью. Ювенильная патология является наследственной болезнью центральной нервной системы, которая передается генетически при помощи аутосомно-рецессивных механизмов. Наследственный характер является главным отличием ювенильной патологии от стандартной болезни Паркинсона, которая обусловлена мультифакторной этиологией. После открытия в 1998 году гена Паркина, внедрение в медицину методик ДНК-диагностики дефектов данного гена позволило специалистам выявлять случаи ювенильного паркинсонизма гораздо чаще. Распространенность данной патологии не имеет территориальных ограничений, в плане половой принадлежности – чаще она встречается у женщин.
Паркинсонизм с ранним началом – это заболевание, которое выявляется у лиц до 45 лет, чаще всего обусловленное генетическими факторами. Установлена ассоциация болезни Паркинсона с некоторыми генными полиморфизмами детоксикации ксенобиотиков, в системе антиоксидантной клеточной защиты, при метаболизме дофамина, в процессе липидного обмена. При выявлении носительства аллельных генов риск развития болезни Паркинсона в организме повышается, возникает наследственная предрасположенность к патологии. Комбинация неблагоприятных полиморфизмов провоцирует раннюю манифестацию заболевания
Важно понимать, что именно в молодом возрасте причинами болезни Паркинсона чаще всего становятся генные предрасположенности, в то время как в пожилом данную патологию чаще провоцируют средовые и прочие факторы
Патологией с поздним дебютом принято считать болезнь Паркинсона, которая возникает после 85 лет, не проявляясь при этом ранее никакими признаками.
По проявлениям заболевания
В зависимости от проявлений и симптоматики болезни рассматриваемую патологию можно подразделить на:
- дрожательную форму, для которой весьма характерен тремор головы, конечностей, нижней челюсти с высокой или средней амплитудой, а также повышенным (иногда нормальным) тонусом мышечной ткани;
- дрожательно-ригидную форму, при которой тремор возникает в дистальных отделах конечностей и в ходе прогресса болезни присоединяется скованность при произвольных движениях;
- акинетико-ригидную форму (самую неблагоприятную из всех), при которой активность движений пациента резко падает, часто доходя до обездвиженности, а тонус мышц резко повышается, что грозит возникновением мышечной контрактуры;
- смешанную форму, при которой все вышеперечисленные формы могут проявляться как совместно, так и перетекать одна в другую;
- атипичную форму, которой характерны синуклеинпатии (деменция с тельцами Леви, идиопатический паркинсонизм и другое) либо таупатии (кортико-базальная деменция, супрануклеарный парез взора и другое).
Каждая форма болезни Паркинсона, помимо различия в проявлениях, может требовать специфической терапии и ухода за пациентом.
Причины
Основная причина заболевания – это отмирание нейронов в области головного мозга, которая отвечает за координированное действие мышц и мышечный тонус. Также отметили недостаток дофамина в этой области мозга, который вызывает такие симптомы, как тремор и мышечная скованность. А вот факторов риска или предпосылок довольно много. Они не обязательно напрямую приводят к развитию заболевания, но значительно повышают его вероятность.
Выявить точную причину может только врач-невролог после полноценного обследования.
Наши врачи

Панков Александр Ростиславович
Врач-невролог
Стаж 40 лет
Записаться на прием

Новикова Лариса Вагановна
Врач-невропатолог, кандидат медицинских наук, врач высшей категории
Стаж 39 лет
Записаться на прием
Диагностика
Стоимость: 14 000 руб.
Подробнее
Сначала врач собирает анамнез. Пациенту задают такие вопросы:
- Как давно появились первые симптомы и как быстро они прогрессировали?
- Усиливается ли тремор в покое?
- Есть ли наследственные предпосылки к развитию заболевания?
- Работает ли пациент на производствах с повышенной токсической опасностью?
- Принимает ли пациент лекарственные препараты, повышающие риск развития паркинсонизма?
- Были ли в недавнем прошлом тяжелые эпизоды инфекционных заболеваний?
- Были ли травмы головы?
Затем врач проводит стандартный для подобных жалоб неврологический осмотр: оценивает походку, мышечный тонус, характер тремора и т.д.
Следующий этап – фармакологический тест. Он заключается в назначении пациенту препарата на основе дофамина или аналогичных веществ. Если есть паркинсонизм, то это способствует снижению симптоматики.
Нередко требуется консультация психолога для оценки когнитивной и эмоциональной сферы. Обычно для этого используют стандартные тесты и опросники.
Подтвердить диагноз можно на – обследование покажет патологические участки в области, отвечающей за мышечный тонус и координацию. Эти высветленные участки показывают отмершие нейроны. МРТ позволяет также подтвердить или исключить опухоль.
Диагностика заканчивается постановкой диагноза, в соответствии с которым назначают лечение.
Лечение паркинсонизма
Лечение сходно и для синдрома Паркинсона, и для болезни Паркинсона. Главное отличие заключается в том, что при синдроме требуется установить причину и начать лечение основного заболевания.
Рекомендуются следующие методы лечения:
- Назначаются препараты с содержанием дофамина или его предшественников.
- Препараты, которые тормозят разрушение дофамина.
- Нейропротекторы – защищают нейроны от гибели.
- Антидепрессанты – при серьезных нарушениях эмоциональной сферы.
- Лечебная физкультура – способна снизить симптоматику на ранних стадиях.
- Методика глубокой стимуляции мозга – применяется не повсеместно, но дает хорошие результаты. Метод заключается в ношении устройства, от которого в мозг идут электроды, стимулирующие соответствующий участок мозга.
Эффективность медикаментозного лечения оценивают по снижению симптоматики. Если консервативная терапия оказалась неэффективной, то назначают хирургическое вмешательство.
Оперативное лечение: к нему прибегают при неэффективности медикаментозного. Операция называется стереотаксической деструкцией ядер таламуса и заключается в разрушении области мозга, отвечающей за чувствительность. Процедура позволяет снизить симптоматику и вернуть способность к нормальному движению.
В клинике ЦЭЛТ работают квалифицированные неврологи, которые предлагают терапию синдрома Паркинсона. Современные методы диагностики позволяют врачам точно установить причину болезни, а многолетний опыт – назначить максимально эффективное лечение.
- Рассеянный склероз
- Мышечная дистония
Лечение болезни Паркинсона
Это заболевание является неизлечимым, все современные препараты для терапии только облегчают симптомы болезни Паркинсона. Симптоматическое лечение направлено на устранение двигательных нарушений.
Как лечить болезнь Паркинсона? На ранних стадиях заболевания показана посильная физическая нагрузка, лечебная физкультура. Лечение препаратами следует начинать как можно позже, поскольку при длительном многолетнем приеме медикаментов у больного развивается привыкание, вынужденное повышение дозировки и как следствие усиление побочных эффектов.
- При выраженных клинических проявлениях паркинсонизма в настоящее время базисным препаратом является леводопа, обычно в сочетании с ингибитором декарбоксилазы. Дозы увеличивают медленно, в течение нескольких недель, до получения клинического эффекта. Побочные действия препарата – дистонические нарушения и психозы. Леводопа, попадая в ЦНС, декарбоксилируется в допамин, необходимый для нормальной функции базальных ганглиев. Препарат влияет прежде всего на акинезию и в меньшей степени – на другие симптомы. При сочетании леводопы с ингибитором декарбоксилазы можно уменьшить дозу леводопы и тем самым уменьшить риск развития побочных явлений.
- В арсенале симптоматических антипаркинсонических средств большое место занимают холинолитические препараты, которые, блокируя м– и н-холинорецепторы, способствуют расслаблению поперечнополосатой и гладкой мускулатуры, уменьшают насильственные движения и явления брадикинезии. Это естественные и синтетические атропиноподобные препараты: беллазон (ромпаркин), норакин, комбипарк. Применяют также препараты фенотиазинового ряда: динезин, депаркол, парсидол, дипразин. Основная причина многообразия медикаментозных препаратов, используемых для лечения паркинсонизма, в недостаточной их лечебной эффективности, наличии побочных явлений, индивидуальной непереносимости и быстром привыкании к ним.
- Морфологические и биохимические изменения при болезни Паркинсона настолько сложны, а течение заболевания и его последствия настолько тяжелы, а еще и усугубляются эффектами заместительной терапии — леводопой, что лечение таких больных считается верхом врачебного мастерства и подвластно виртуозам – неврологам. Поэтому открыты и работают специальные центры по лечению паркинсонизма, где уточняется диагноз, ведется наблюдение, подбираются дозы необходимых препаратов и схемы лечения. Самостоятельно назначать и принимать препараты нельзя.
Для заместительной терапии используют леводопу, карбидопу, наком. Стимулирует выброс дофамина адамантин, мемантин, бромкриптин, тормозят процесс обратного захвата допамина – антихолинэстеразные препараты и трициклические антидепрессанты (амитриптиллин), тормозит процесс распада дофамина селегилин, нейропротекторами ДА- нейронов используются антиоксиданты – селегилин, токоферол, блокаторы кальциевых каналов – нифидипин.
На ранних стадиях для сохранения качества жизни доказано применение прамипексола (мирапекса). Он является препаратом первой линии лечения болезни паркинсона с высоким уровнем эффективности и безопасности. В лечении используется юмекс, неомидантан, нейропротекторы, антиоксиданты. Больным необходима лечебная гимнастика по индивидуальной программе – как можно больше двигаться и дольше сохраняться активными.
Источники
- Tucker HR., Mahoney E., Akhtar K., Kao TJ., Mamone G., Mikkilineni S., Ravi M., Watkins H., Terrelonge DL., Martin C., Unger K., Kim G., Fiber K., Gupta M., Indajang J., Kochman EM., Sachs N., Feustel P., Molho ES., Pilitsis JG., Shin DS. Motor Thalamic Deep Brain Stimulation Alters Cortical Activity and Shows Therapeutic Utility for Treatment of Parkinson’s Disease Symptoms in a Rat Model. // Neuroscience — 2021 — Vol460 — NNULL — p.88-106; PMID:33631218
- Cotterell P. Parkinson’s disease: symptoms, treatment options and nursing care. // Nurs Stand — 2018 — Vol33 — N7 — p.53-58; PMID:30198239
Диагностика
Раннее диагностирование болезни Паркинсона помогают выявить патологию на самых ранних стадиях. Превентивные анализы и проверки рекомендованы людям, у которых в семейный анамнез включает большое число случаев выявления неврологических заболеваний. В медицинской практике это так и называется неврологический анамнез».
Ранняя диагностика избавит пациента от обращения к специалисту уже только на стадии выраженных внешних нарушений. Дополнительные обследования на поздней стадии уже не требуются.
В перечень вариантов ранней диагностики входит:
- проведение осмотра;
- выполнение обонятельного теста, нарушение обоняния становится одним из первых выраженных проявлений;
- мигреней;
- в ходе личной беседы врач уточняет качество сна, уровень раздражительности.
Анализы выявить присутствие этого неврологического нарушения не в состоянии. В ситуации присутствия в семье неврологического анамнеза требуется тщательно контролировать наличие или отсутствие первых проявлений в виде минимального тремора, болей между лопатками.
Подтверждение диагноза проводится с помощью использования КТ или МРТ. Часто именно проведение таких исследований, например, после травмы головы или при исследовании гайморовых пазух, позволяют определить патологические нарушения еще до первых внешних проявлениях.